
题目列表(包括答案和解析)
25.(10分)从某铝镁合金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。
(1)自反应开始到反应结束,从小烧杯中可观察到的主要现象。(请依次写出)
(2)开始时产生气泡的速率较慢的原因是 。
后来的反应速率相当快的原因是 。
(3)写出所形成的原电池的负极材料名称:
和电极反应式:
(4)欲利用该反应来测定合金中铝的含量,还应测定的数据。(请逐一写出)
24.(8分)工业上采用Fe、C为电极电解K2MnO4溶液制KMnO4.
(1)电解时,应以 作阴极,电解过程中阴极附近溶液pH将会
(2)阳极反应式为 (3)总电解反应式为
23.(10分)如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下问题:
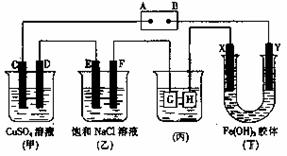
(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式是______________________ ___。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______________。
(4)欲用丙装置给铜镀银,G应该是_______,电镀液的主要成分是_________(填化学式)。
22.(8分)在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答:

(1)加水前导电能力为零的理由是:
(2)a、b、c、d四点醋酸的电离度大小顺序是 (3)a、b、c、d四点溶液PH值大小顺序是 (4)若要把b点溶液中(CH3COO-)、(OH-)均减小,可采用的方法是 (选择正确的选项) (A)加水 (B)加NaOH (C)加H2SO4 (D)加Na2CO3
21.(4分)已知HCO3-比HBrO更难电离,但HBrO的酸性比H2CO3弱,写出以下反应的离子方程式: (1)向NaHCO3溶液中滴加少量溴水:
(2)向Na2CO3溶液中滴加少量溴水:
20.已知:
① CH4 ( g )+4NO2( g )=4NO( g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
② CH4 ( g )+4NO( g )=2N2( g )+CO2( g )+2H2O( g ) △H=一1 160 kJ·mol一1。
下列正确的选项是
A.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( l) △H=一867 kJ·mol-1
B.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=一867 kJ·mol-1
C.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=一586kJ·mol-1
D.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g) △H=+586kJ·mol-1
19.将0.l mol∙L-1的下列物质的水溶液,从常温加热到80℃,溶液的pH不变的是
A.NaCl B. NaOH C.H2SO4 D. NH4Cl
18.在相同温度和压强下,对反应CO2(g)+3H2(g) CH3OH(g)+H2O (g)进行甲、乙、 丙、丁四组实验,,实验起始时放入容器内各组分的物质的量见下表k*s5u
CH3OH(g)+H2O (g)进行甲、乙、 丙、丁四组实验,,实验起始时放入容器内各组分的物质的量见下表k*s5u
|
物质的量 |
CO2 |
H2 |
CH3OH(g) |
H2O |
|
甲 |
a
mol |
a
mol |
0
mol |
0
mol |
|
乙 |
2a mol |
a
mol |
0
mol |
0
mol |
|
丙 |
0
mol |
0
mol |
a
mol |
a
mol |
|
丁 |
a
mol |
0
mol |
a
mol |
a
mol |
上述四种情况达到平衡后,n(CH3OH)最大的是
A.甲 B.乙 C.丙 D.丁
17.分别在PH=1的酸溶液和PH=14的NaOH溶液中加入足量的铝,放出氢气的量前者多,其原因可能是:①两溶液的体积相同,而酸是多元强酸;②两溶液的体积相同,酸是弱酸;③酸溶液的体积比NaOH溶液体积大;④酸是强酸,且酸溶液的浓度比NaOH溶液浓度大;其中正确的为 A.只有②和③ B.只有②和④ C.只有①和③ D.只有①
16.用标准盐酸滴定未知浓度的NaOH溶液时,下列操作能引起偏低误差的是 A.锥形瓶用待测液润洗2~3次 B.指示剂变色后又立即就停止滴定 C.滴定前酸式滴定管俯视读数,滴定后又仰视 D.滴定结束后,酸式滴定管尖嘴处悬挂一滴液体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com