
题目列表(包括答案和解析)
4.下列关于化学反应限度的叙述错误的是( )
A.不同的化学反应,限度可能不同
B.可以通过改变温度来控制化学反应的限度
C.可以通过改变某反应物的量来改变反应的限度
D.当一个化学反应在一定条件下达到限度时,正,逆反应速率便停止.
3.不能作为元素周期表中元素排列顺序的依据的是( )
A.原子的核电荷数 B.原子的核外电子数
C.原子的质子数 D.原子的中子数
2.下列化学名词正确的是( )
A.三硝基甲笨 B.烧碱 C.乙酸乙脂 D.炭酸钠
1.下列化学电池不易造成环境污染的是( )
A.铅蓄电池 B.锌锰电池 C.氢氧燃料电池 D.镍镉电池
28.(6分)把2.5 mol A和2.5
molB两种气体混合放入容积为2L的密闭容器里发生反应3A(g)+B(g) XC(g)+2D(g),经5S后反应达到平衡,在此5S内C的平均反应速率为0.2mol/(L· s),同时生成1
mol D,试求:
XC(g)+2D(g),经5S后反应达到平衡,在此5S内C的平均反应速率为0.2mol/(L· s),同时生成1
mol D,试求:
⑴在此5S内D的平均反应速率。
⑵达到平衡时B的转化率
⑶计算X的值
27.(12分)某实验小组用下列装置进行乙醇的实验,试回答下列问题:
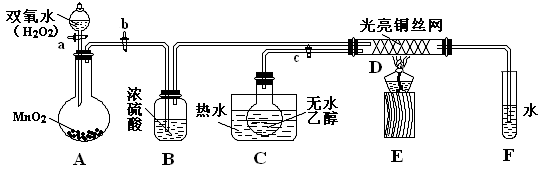
(1)A中发生反应的化学方程式为: ,还可以用 代替 MnO2的作用
(2)实验过程中D处铜丝网有红色和黑色交替出现的现象,请用化学方程式解释原因。
现象①:红色变黑色:
现象②:黑色变红色: 且反应类型:


 (3)在F装置中,由于产物速率不易控制,有可能造成倒吸,所以F装置可改用 装置(填字母)。
(3)在F装置中,由于产物速率不易控制,有可能造成倒吸,所以F装置可改用 装置(填字母)。
a b c
(4)实验室可对E部分采取合理的操作方法以防止安全隐患,请对此提出你的意见:
26.(12分)A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出B元素的离子结构示意图: ,
(2)A的一种化合物和CO2反应有气体生成,写出反应的化学方程式,
(3) 比较C、D、E的最高价氧化物对应水化物的酸性强弱(用化学式表示)
比较A、B、E的离子半径(用离子符号表示)
(4)写出B的氧化物与E最高价氧化物的水化物反应的离子反应式
(5)写出E与C同主族上一周期元素所形成的化合物的电子式的形成过程
25.(8分) (1)下列关于充电电池、干电池的叙述,合理的是
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为
(3)原电池在NaOH介质中,铝为负极,其负极反应式为
(4)一电池反应的离子方程式是 Zn+Cu2+=Zn2+ +Cu,该反应的原电池正极、负极和电解液是
24.(15分)(1)已知有1H216O、D2S、3H218O、S17O2、2H2S、S16O2,其中有__ __种元素, 种核素, 种分子。
(2)结合甲烷、乙烯和苯燃烧的现象,推测烃类在氧气中充分燃烧的规律有 。
①含碳量越高,生成的烟越多;②等质量的烃,耗氧量为:甲烷>乙烯>苯;③等物质的量的烃,耗氧量为:甲烷>乙烯>苯;④含碳量越高,产生的火焰越明亮。
(3)将石蜡油与碎瓷片混合共热,产生的混合气体冷却至室温后,其成分如下:
|
物质 |
CH4 |
CH3-CH3 |
CH2==CH2 |
|
物质的量分数 |
20% |
30% |
50% |
将2 mol该混合气体通入足量的溴的四氯化碳溶液中,消耗Br2的质量为
(4)有机化合物的结构简式可进一步简化,如:
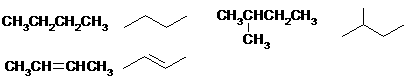 写出下列物质的分子式:
写出下列物质的分子式:
a.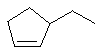 b.
b.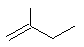
(5)某烃A的分子式为C8H18,其不能由任何C8H16的异构体与氢气加成得到,则该烃A的结
构简式为 ,某烃B的分子式也是C8H18。它可以由而且只能由一种C8H16的异构体与氢气加成得到,则该烃B的结构简式为
23.有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是( )
A.X、M两种元素只能形成X2M型化合物
B.由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低
C.元素Y、Z、W的氢化物稳定性依次增强
D.元素W和M的某些单质可作为水处理中的消毒剂
卷Ⅱ(非选择题,共53分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com