
题目列表(包括答案和解析)
20.在xR++yH++O2=mR3++nH2O的离子反应中,系数m的值为 ( )
A.2x B.4 C.y/2 D.2
答案:CD[提示:根据质量守恒可知n=2,且y=4,然后再由电荷守恒和质量守恒可 得x=m和x+4=3m,m=2]
19.下列反应的离子方程式中,书写正确的是 ( )
A.氢氧化铁和盐酸反应:Fe(OH)3+3H+=Fe3++3H2O
B.硝酸银溶液和盐酸反应:Ag++HCl=AgCl↓+H+
C.硫酸铜和氢氧化钠溶液反应:Cu2++OH=Cu(OH)2↓
D.碳酸氢钠受热分解:HCO-3=CO2↑+H2O
答案:A[提示:B中HCl为强电解质,应拆写成离子形式;C项质量不守恒;D项 NaHCO3受热分解不属于离子反应]
18.已知有如下反应:
(1)2BrO-3+Cl2=Br2+2ClO-3
(2)ClO-3+5Cl-+6H+=3Cl2↑+3H2O
(3)2FeCl3+2KI=2FeCl2+2KCl+I2
(4)2FeCl2+Cl2=2FeCl3
下列粒子氧化性由强到弱的顺序正确的是 ( )
A.BrO-3>ClO-3>Cl2>Fe3+>I2
B.ClO-3>BrO-3>Cl2>Fe3+>I2
C.BrO-3>Cl2>ClO-3>I2>Fe3+
D.BrO-3>ClO-3>Fe3+>Cl2>I2
答案:A[提示:在氧化还原反应中,氧化剂的氧化性比氧化产物的氧化性强,由此可 知:(1)中BrO-3>ClO-3;(2)中ClO-3>Cl2;(3)中Fe3+>I2;(4)中Cl2>Fe3+.即 氧化性BrO-3>ClO-3>Fe3+>I2,A正确]
17.要检验某溶液中是否含有Cl-,可选用的试剂是 ( )
A.AgNO3溶液 B.AgNO3溶液和稀盐酸
C.AgNO3溶液和稀硫酸 D.AgNO3溶液和稀硝酸
答案:D
16.已知某溶液中有Na+、Ba2+、Fe2+三种阳离子,那么溶液中的阴离子可能是 ( )
A.SO2-4 B.Cl- C.S2- D.NO-3
答案:BD[提示:本题也属于离子共存问题,由于原溶液中含Ba2+、Fe2+,所以不可能 存在SO2-4和S2-,而可能含有Cl-和NO-3,故应选B、D]
15.下列物质中,既能导电,又属于强电解质的一组物质是 ( )
A.石墨、醋酸溶液、食盐晶体
B.熔融态KOH、盐酸、熔融态氯化钠
C.稀H2SO4、NaOH溶液、CO2
D.液氨、石灰水、水银
答案:B
14.能够说明氯气比单质硫的氧化性强的反应是 ( )
A.CuCl2+H2S=CuS↓+2HCl
B.Cl2+H2S=2HCl+S↓
C.FeS+2HCl=FeCl2+H2S↑
D.NaCl+H2SO4(浓)=NaHSO4+HCl↑
答案:B[提示;在四个反应中,仅B项为氧化还原反应,且Cl2为氧化剂,S为氧化产 物,在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,所以Cl2的氧化 性比S的氧化性强]
13.下列离子组可在同一溶液中大量共存,且形成无色溶液的是 ( )
A.K+、Na+、OH-、Cl- B.Cu2+、Ba2+、NO-3、Cl-
C.Na+、Mg2+、OH-、SO2-4 D.Ba2+、H+、NO3-3、OH-
答案:A[提示:B中Cu2+为蓝色,不符合题意;C中Mg2+会与OH-形成难溶的 Mg(OH)2,不能共存;D中H+与OH-会形成难电离的水,也不能共存.应选A]
12.氢气在氯气中燃烧生成36.5 g氯化氢时,下列叙述中,正确的是 ( )
A.有1 g氧化剂被氧化 B.有35.5 g氯元素被氧化
C.有35.5 g氧化剂被还原 D.有1 g氢元素被还原
答案:C[提示:本题A项说法明显错误,氧化剂应被还原,根据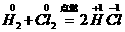 可知H2为还原剂,Cl2为氧化剂,当有36.5g HCl生成时,应该有1 g氢元素被氧化,同时有35.5 g氯元素被还原,即C项正确]
可知H2为还原剂,Cl2为氧化剂,当有36.5g HCl生成时,应该有1 g氢元素被氧化,同时有35.5 g氯元素被还原,即C项正确]
11.在下列反应中,电子转移发生在不同物质中的金属元素之间的是 ( )
A.CuCl2+2NaOH=Cu(OH)2↓+2NaCl
B.Cu+2FeCl3=2FeCl2+CuCl2
C.Fe+2HCl=FeCl2+H2↑
D.AgNO3+NaCl=AgCl↓+NaNO3
答案:B[提示;四个反应中,A、D两项中的反应为非氧化还原反应,无电子转移;B中Cu失去电子,Fe3+得到电子,符合题意;C中电子转移发生在Fe与H+之间]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com