
题目列表(包括答案和解析)
5.少量的金属钠通常保存在
A.水中 B.煤油中 C.氯化钠溶液中 D.盐酸中
4.与原子序数不一定相等的是
A.核电荷数 B.质子数 C.中子数 D.核外电子是
3.元素周期表所具有的列数为
A.16 B.17 C.18 D.19
2. 到目前为止,元素周期表所具有的周期数为
A.一个 B.三个 C.五个 D.七个
1. 制出第一张元素周期表的人是
A.李世光 B爱迪生 C.陈景润 D.门捷列夫
32. (4分)在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+ 3N(g) x Q(g)+3R(g),经2min后,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
(4分)在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+ 3N(g) x Q(g)+3R(g),经2min后,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
(1)用气体M来表示该反应的化学反应速率是多少?
(2)x的值是多少?
31.(6分)
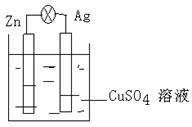 (1)将锌片和银片浸入硫酸铜溶液中
(1)将锌片和银片浸入硫酸铜溶液中
组成原电池。
锌片上发生的电极反应:____________;
银片上发生的电极反应:____________。.
(2)若该电池中两电极的原总质量为160 g,工作
一段时间后,取出锌片和银片洗净干燥后称重,
总质量为158 g。
试计算:原电池中正极的质量是增加还是减小,
变化值是多少?
30. (每空2分,共10分)某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
|
实验步骤 |
向3-4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
|
实验现象 |
产生白色沉淀 |
|
离子方程式 |
(1)
|
|
小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
|
假设出现的实验现象,说明理由 |
假设:Ⅰ 无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2) ,理由:(3) |
|
证明你的假设 |
现象:产生大量的白色沉淀 |
|
离子方程式 |
(4)
|
|
解释 |
(5)
|
29.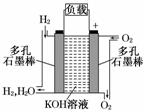 (每空2分,共10分)右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从两极通入燃料电池时,便可在闭合回路中不断地产生电流.这被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。
(每空2分,共10分)右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从两极通入燃料电池时,便可在闭合回路中不断地产生电流.这被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。
试回答下列问题:
(1)图中通过负载的电子流动方向______(填“向左”或“向右”),负极发生 反应(填“氧化”或“还原”)
(2)写出氢氧燃料电池工作时电极反应方程式和总反应方程式.
负极:_______________________ ,正极:___________________________,
总反应:________________________.
28.(每空2分,共10分) A、B、C、D、E五种短周期元素的原子序数依次增大,上述元素中只有一种金属元素。A、B同周期,化合物AB2、DB2均是可使澄清石灰水变浑浊的气体。又已知C、E的单质均可溶于NaOH溶液,且C与NaOH溶液反应可产生气体。
(1)写出A、E元素的名称:A E________
(2) 画出C原子的原子结构示意图
(3)写出DB2使澄清石灰水变浑浊的化学方程式:_____________________
(4)写出E的单质与NaOH溶液反应的离子方程式: ______________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com