
题目列表(包括答案和解析)
15.a、b、c、d四块金属片浸入稀硫酸中,用导线分别两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时,d表面发生还原反应;a、c相连时c极上产生大量气泡;b、d相连时d质量减轻。则四种金属的活动性顺序由强到弱为
A.a>b>c>d B.c>a>b>d C.b>d>c>a D.a>c>d>b
14.下列有关离子化合物的叙述不正确的是
①典型离子化合物一定是只含有离子键的化合物 ②离子化合物中可能不存在金属元素;③离子化合物熔点很高,加热一定难分解 ④离子化合物中可能含有共价键。
A.①② B.②③ C.①③ D.②④
13.一定质量的锌和足量的稀硫酸反应时,加入少量CuSO4固体,下列叙述正确的是
A.反应速率减慢,产生H2的量不变 B.反应速率加快,产生H2的量不变
C.反应速率不变,产生H2的量增加 D.反应速率加快,产生H2的量减少
12.下列各组顺序的排列不正确的是
A.原子半径:Na<Mg<Si B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H2SiO3<H2CO3<HNO3 D.熔点: NaCl>S > CO2
11.X、Y、Z和R分别代表四种元素。如果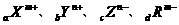 四种离子的电子层结构相同(a、b、c、d为元素的原子序数),则下列关系正确的是
四种离子的电子层结构相同(a、b、c、d为元素的原子序数),则下列关系正确的是
A.  B.
B.
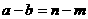
C.  D.
D.
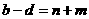
10. Na2S2O3溶液跟稀H2SO4反应:Na2SO3+H2SO4=
Na2SO4+SO2↑+S↓+H2O
Na2S2O3溶液跟稀H2SO4反应:Na2SO3+H2SO4=
Na2SO4+SO2↑+S↓+H2O
下列各组实验中,溶液中最先变浑浊的是
|
|
反应 |
反 应 物 |
H2O |
|||
|
|
温度 |
Na2S2O3 |
H2SO4 |
V |
||
|
|
℃ |
v(mL) |
c(mol×L-1) |
v(mL) |
c(mol×L-1) |
(mL) |
|
A |
10 |
5 |
0.1 |
5 |
0.1 |
20 |
|
B |
10 |
5 |
0.1 |
10 |
0.1 |
15 |
|
C |
30 |
5 |
0.1 |
10 |
0.1 |
15 |
|
D |
30 |
10 |
0.1 |
10 |
0.1 |
10 |
9. 如右图所示的装置中,a的金属性比氢要强,b为碳棒。
如右图所示的装置中,a的金属性比氢要强,b为碳棒。
有关此装置的下列叙述不正确的是
A.一段时间后振荡溶液,溶液pH变大
B.a是负极,b是正极
C.导线中有电子流动,外电路中,电流从a极到b极
D.a 极上发生了氧化反应
8.下列有关浓硝酸和浓硫酸的叙述正确的是
A.常温下都能与铜较快反应 B.受热都易分解
C.露置于空气中,溶液质量均减轻 D.常温下都可用铁制容器贮存
7.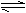 在A(g)+2B(S) 2C(g)+3D(g)反应中,表示该反应速率最快的是
在A(g)+2B(S) 2C(g)+3D(g)反应中,表示该反应速率最快的是
A.v(B)= 3 mol/(L· min) B.v(A)=0.02mol/(L· s)
C.v(C)= 2.5 mol/(L· min) D.v(D)=0.06mol/(L· s)
6. 某金属元素M的最高价氧化物化学式为M2O3,式量102,电子数为50,已知氧原子
核内有8个中子,M原子核内中子数是
A. 13 B. 14 C.21 D. 27
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com