
题目列表(包括答案和解析)
5. 下列物质属于离子化合物的是
A.C60 B.HCl C. C6H6 D.CaCl2
4.下列各组中化合物的性质比较,不正确的是
A.酸性:HClO4>H2SO4>H3PO4 B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S> HCl D.非金属性:O>C>Si
3.下列各组物质中,不互为同素异形体的是
A.金刚石和C60 B.红磷和P4 C.O2和O3 D. 1H和2H
2. 下列表示物质结构的化学用语或模型正确的是
下列表示物质结构的化学用语或模型正确的是
 A.乙烯的结构简式:CH2CH2 B.CH4分子的比例模型:
A.乙烯的结构简式:CH2CH2 B.CH4分子的比例模型:
C.溴化钠的电子式: 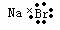 D.Cl-离子的结构示意图:
D.Cl-离子的结构示意图:
1.2011年3月11日,日本9级大地震导致福岛核泄漏,主要泄露放射性同位素为131 53I ,碘131被人体吸入会引发甲状腺疾病,该核素的中子数和质子数之差为
A.131 B.25 C.53 D.21
31.(8分)A、B、C、D 、E 5种短周期元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C;C、E 同主族.
(1) B在周期表中的位置第______周期,第_______族;
(2) C、E 两种元素可能形成化合物的化学式_______________________;
(3)化合物BC与C2反应的化学方程式
____________________________________________________________;
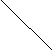
30.(16分)下表是元素周期表的一部分,请回答有关问题:
|
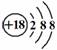
(1) 表中化学性质最不活泼的元素,其原子结构示意图为
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该两性氢氧化物与⑦的氢化物的水溶液反应的离子方程式
(3)④元素与⑦元素形成的化合物的电子式为 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填酸的化学式)
(5)③元素与⑩元素两者核电荷数之差是 。
(6)④⑤两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是 (填编号)。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
29. (12分)一定温度下在10L容器中加入5molSO2和3molO2,当反应达到平衡时,有3molSO2发生了反应,则:
(1)生成了 molSO3,SO2的转化率为 (用百分数表示)。
(2)平衡时容器内气体的总物质的量为 。
(3)平衡时SO2的浓度是 ,O2的浓度是 ,
SO3的浓度是 。
28.下列各分子中所有原子都满足最外层为8电子结构的是
A.BeCl2 B.NH3 C.PCl5 D.N2
第II卷(非选择题,共44分)
注意:第Ⅱ卷答在答题纸上,将第3页撕开,只交答题纸
27.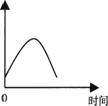 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示。在下列因素中对产生H2速率有影响的是:
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示。在下列因素中对产生H2速率有影响的是:
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com