
题目列表(包括答案和解析)
16.测得某溶液中含Cu2+、K+、SO2-4、Cl-四种离子,且阳离子的物质的量之比为n(Cu2+):n(K+)=3:4,则SO2-4与Cl-的个数比可能是 ( )
A.3:2 B.1:4 C.1:8 D.2:5
答案:C[提示:设n(Cu2+)=3mol,则n(K+)=4 mol,SO2-4、Cl-的物质的量分别为 x mol,y mol,由电荷守恒有2x+y=3×2+4×1,讨论x,y的取值并与选项对比可知,只有C项符合题意]
15.血红蛋白的相对分子质量为68000,已知其中含铁0.33%,则平均每个血红蛋白分子中铁的原子数为 ( )
A.5 B.4 C.3 D.2.408×1024
答案:B
14.空气和二氧化碳按体积比5:1混合,将混合气体与足量的红热焦炭充分反应,设空气中氮气和氧气的体积比为4:1,不计其他成分,且气体体积都在同温、同压下测定,则反应后的气体中一氧化碳的体积分数为 ( )
A.20% B.43% C.50% D.100%
答案:C[提示:混合气体的变化过程为:
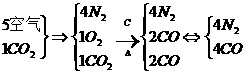 故选C项]
故选C项]
13.两份体积相同的某植物营养液,其配方如下表所示,则两份营养液的成分 ( )
 含量 成分
含量 成分编 号 |
KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
|
① |
0.3mol |
0.2mol |
0.1mol |
- |
|
② |
0.1mol |
0.3mol |
- |
0.1mol |
A.仅c(K+)相同 A.仅c(Cl-)相同
C.完全相同 D.完全不同
答案:C[提示:由n1+n2+…=n(总)可知,两份营养液中各离子的物质的量均相等]
10.配制0.5 mol/L NaOH溶液250 mL,在下列仪器中:①托盘天平;②量筒; ③烧杯;④玻璃棒;⑤漏斗;⑥500mL容量瓶;⑦药匙;⑧250 mL容量瓶;⑨胶头滴管;⑩坩埚,需要用到的仪器为 ( )
A.①③④⑥⑨⑩ B.①④⑦⑧⑨⑩
C.①③④⑦⑧⑨ D.①②④⑤⑧⑨
答案:C[提示:由用固体物质配制一定物质的量浓度溶液的实验操作可知,C项正确] 11.由锌、铁、铝、镁四种金属中的两种组成的12 g混合物与足量的盐酸反应,产生的H2在标准状况下为11.2 L,则混合物中一定含有的金属是 ( )
A.锌 B.铁
C.镁 D.铝
答案:D[提示:由平均值法可知,产生11.2 L H2时,消耗金属质量大于12 g的有两种Zn、Fe,而消耗金属质量小于12g的只有Al,故D项正确] 12.将0.1mol/L K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和纯水混合,要使混合溶液中K+、Al3+、SO2-4的浓度分别为0.1 mol/L,0.1 mol/L,0.2 mol/L,则所取K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比是 ( )
A.1:1:1 B.2:2:1
C.1:1:2 D.2:1:1
答案:D[提示:由题意知,V(K2SO4)=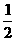 V(总),V[Al2(SO4)3]=
V(总),V[Al2(SO4)3]= 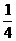 V(总),故只有 D项符合]
V(总),故只有 D项符合]
9.在标准状况下,560体积的氨气溶于1体积的水中,测得氨水的密度为0.9 g/cm3,则氨水的物质的量浓度为 ( )
A.1.58 mol/L B.31.6 mol/L C.15.8 mol/L D.18 mol/L
答案: C[提示:由物质的量浓度定义可得
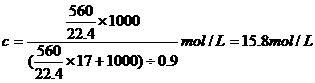 ]
]
8.在同温、同压下,气体A的质量与气体B的质量相等,但气体A的体积小于气体B的体积,则气体A的相对分子质量和气体B的相对分子质量的关系是 ( )
A.M(A)>M(B) B.M(B)>M(A)
C.M(B);M(A) D.无法比较
答案:A[提示;由题意知ρA>ρB,故由阿伏加德罗定律的推论可知A项正确]
7.NA表示阿伏加德罗常数,下列叙述中,不正确的是 ( )
A.4℃时,5.4 mL水中所含水分子数为0.3NA
B.2 L 1 mol/L硫酸钾溶液中钾离子的总数为3NA
C.标准状况下,22.4L甲烷和乙炔的混合物中所含的分子数为NA
D.1 mol甲烷的质量与NA个甲烷分子的质量之和相等
答案:B[提示:因4℃时水的密度ρ=1 g/cm3,所以5.4 mL水的质量为5.4 g,物质的量为0.3mol,故A项正确;2 L 1 mol/L K2SO4溶液中K2SO4的物质的量为2mol,故钾离子的总数为4 mol,故B项不正确;由气体摩尔体积及摩尔质量的定义可知,C、D两项是正确的]
6.2 g AO2-3中,核外电子数比质子数多3.01×1022个,则元素A的相对原子质量为( )
A.12 B.32
C.60 D.80
答案:B[提示:因为每个AO2-3中,核外电子数比质子数多2个,所以有AO2-3电子数比质子数多(M为AO2-3的摩尔质量)
M 2mol
2g 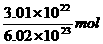
得M=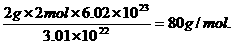
故A的相对原子质量为80-3×16=32]
5.某Al2(SO4)3溶液VmL中含a g Al3+,取出mL溶液稀释成4V mL后,溶液中SO2-4的物质的量浓度为 ( )
A. 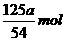 B.
B. 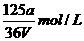 C.
C. 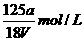 D.
D. 
答案:B[提示:V mL溶液中n(Al3+)=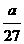 mol,所以
mol,所以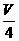 mL溶液中Al3+的物质的量为
mL溶液中Al3+的物质的量为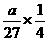 mol,稀释成4V mL溶液后,Al3+物质的量浓度为
mol,稀释成4V mL溶液后,Al3+物质的量浓度为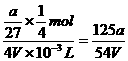 mol/L,所以c(SO2-4)=
mol/L,所以c(SO2-4)=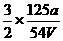 mol/L=
mol/L=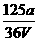 mol/L]
mol/L]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com