
题目列表(包括答案和解析)
3.1 g N2中含a个分子,则阿伏加德罗常数为 ( )
A.  a B.a
C.28a D.
a B.a
C.28a D. 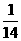 a
a
答案:C[提示:因1 gN2中含a个分子,而1 mol N2的质量为28g,故1 mol N2含28a个分子,所以28a为阿伏加德罗常数的值]
2.对相同质量的SO2和SO3来说,下列关系中,正确的是 ( )
A.含氧原子的个数比为2:3 B.含硫元素质量比为1:1
C.含氧元素质量比为5:6 D.含分子数之比为1:1
答案:C[提示:由于等质量的SO2和SO3的物质的量之比为=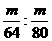 =5:4,故二者中氧原子的个数比为5×2:4×3=5:6,硫原子的个数比(等于质量比)为5:4;含分子数之比为5:4,故C项正确]
=5:4,故二者中氧原子的个数比为5×2:4×3=5:6,硫原子的个数比(等于质量比)为5:4;含分子数之比为5:4,故C项正确]
1.下列叙述中,正确的是 ( )
A.镁的原子质量就是镁的相对原子质量
B.一个铁原子的实际质量约等于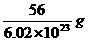
C.水的相对分子质量等于18 g
D.1 mol二氧化硫的质量是64g/mol
答案:B[提示:镁的相对原子质量是镁的原子质量与C的原子质量的1/12的比值,故项不正确;1 mol铁原子的质量为56g,1 mol铁中含阿伏加德罗常数个铁原子,故B项正确;水的相对分子质量应为18,1 mol水的质量才是18 g,故C项不正确; 1 mol SO2的质量为64 g,64g/mol是SO2的摩尔质量,故D项不正确]
4.加强实验的学习.
本章虽然实验内容不多,但对实验的定量要求却是比较高的.要理解实验原理,学习实验步骤,规范实验操作,提高实验技能.
3.学习目标梯度化.
由于本章概念多,又比较抽象,对有些概念,限于接受能力,不要求中学生对这部分内容理解透彻;但总的学习目标不能降低,要在以后对有关章节的学习中逐渐深入地理解有关物质的量的知识,直至达到准确、灵活地应用的目的.
2.以直观表抽象,以比较辨是非.
对于本章学习难度较大的一些概念,要结合一些比喻和直观教具,尽量将抽象的概念形象化,以帮助理解和记忆.对于容易混淆的概念,要通过对比,找出它们之间的区别与联系.
1.重视新旧知识的密切联系.
本章中的知识,虽然概念较多,但与初中化学和高一化学前两章的知识有着密切的联系,本章知识之间的联系就更密切了,因此,在学习的过程中要自觉主动地进行新旧知识之间的联系,以降低新知识点学习的难度,不断地建立、完善知识网络,提高学习效率.
3.本章重点:物质的量及其单位--摩尔;气体摩尔体积和物质的量浓度的概念;有关物质的量浓度概念的计算.
本章难点:物质的量及其单位--摩尔.
2.本章的内容分为三节.按照知识的内在联系,这三节的内容是一个不可分割的整体.本章的第一节着重介绍物质的量及其单位以及摩尔质量,后两节介绍气体摩尔体积和物质的量浓度,并分别讨论了有关物质的量的计算.教材有计划地将与物质的量有关的比较复杂的计算分散到后面的章节中逐步进行介绍,这样做的目的是既减轻了学习本章知识时的负担,又有利于加深理解、巩固和运用有关的概念,特别是可以深化对物质的量及其单位的认识.
1.物质的量是国际单位制中七个基本的物理量之一,物质的量是中学化学中的一个很重要的基本概念,它贯穿于整个高中化学的始终,特别是在化学计算中更是处于核心地位;因此,学好物质的量及其单位,不仅能直接帮助学生理解本章中所讲授的有关摩尔质量、气体摩尔体积、物质的量浓度等知识,而且为在以后的学习中运用这些概念来学习新的知识,以及为进行较复杂计算等打下一定的基础;由于物质的量及其单位在中学化学中占有重要的地位,因此,关于物质的量及其单位的学习不仅是本章的重点,也是整个中学化学的学习重点之一.
通过对本章内容的学习,我们会在微观粒子和宏观物质之间架起一座“桥梁”,这在中学化学,乃至整个科学研究和工农业生产中都有非常重要的意义.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com