
题目列表(包括答案和解析)
16.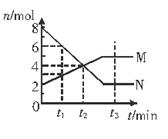 在一定温度下,容器内某一反应中 M 、N 的物质的量随反时间变化的曲线如右图,下列表述中不正确的是(已知t1时,M的纵坐标为3)
在一定温度下,容器内某一反应中 M 、N 的物质的量随反时间变化的曲线如右图,下列表述中不正确的是(已知t1时,M的纵坐标为3)
A.反应的化学方程式为:2N 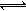 M
M
B.t2时,正反应速率大于逆反应速率,未达到平衡
C.t3时,正反应速率等于逆反应速率,N 和 M 的
浓度相等
D.t1时,N 的浓度是 M 浓度的 2倍
南充高中高2010级期中考试化学试题(理科)
第Ⅱ卷(非选择题,共52分)
15.在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:
3A(g)+B(g)  2C(g)+xD(g),10
min达到化学平衡,生成了2 mol C,经测定
2C(g)+xD(g),10
min达到化学平衡,生成了2 mol C,经测定
D的平均反应速率为0.05 mol·L-1·min-1。下列判断正确的是
A.平衡时A的浓度为1.50 mol·L-1
B.x=1
C.达到平衡时,在相同温度下容器内混合气体的压强是反应前的0.8倍
D.B的转化率为20 %
14.向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时, 按正反应速率由大到小的顺序排列,正确的是
①500 ℃, 10 mol SO2和5 mol O2反应
②500 ℃, 用V2O5作催化剂, 10 mol SO2和5 mol O2反应
③450 ℃, 8 mol SO2和5 mol O2反应
④500 ℃, 8 mol SO2和5 mol O2反应。
A.①②③④ B.②①③④ C.②①④③ D.④③②①
13.将锌片和铜片用导线连接后放入硫酸铜溶液中,发生原电池反应(反应前后溶液体积不变),在反应过程中,下列叙述错误的是
A.电子由锌片经导线流向铜片 B.铜片作正极,锌片作负极
C.溶液中SO42- 的物质的量浓度保持不变 D.溶液中Cu2+移向负极
12.对于放热反应:H2 + Cl2 2HCl ,下列说法不正确的是
A.1 mol H2 的能量高于2 mol H具有的总能量
B.反应物所具有的总能量高于生成物所具有的总能量
C.断开1 mol H-H键和断开1 mol Cl-Cl键所吸收的总能量小于形成2 mol H-Cl键所放出的总能量
D.该反应中,化学能部分转变为热能
11.一定温度下,在恒容的密闭容器中发生反应:A(s)+2B(g)
 C(g)+D(g),当满足下列条件时,不能表明该反应已达到化学平衡状态的是
C(g)+D(g),当满足下列条件时,不能表明该反应已达到化学平衡状态的是
A.v正(B)=2v逆(C) B.混合气体的密度不再变化
C.混合气体的压强不再变化 D.B的物质的量浓度不再变化

10.在一定条件下,RO与R-可发生反应 :RO+5R-+6H+=3R2+3H2O,下列关于R元素的叙述中,正确的是
A.元素R位于周期表中第ⅤA族
B.RO中的R只能被还原
C.R2在常温常压下一定是气体
D.若1 mol RO参与该反应,则转移的电子的物质的量为5 mol
9.右下表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是
A.C的氢化物的水溶液显酸性
B.简单离子半径:B>D
C.B单质在足量A单质中燃烧可生产BA3
D.B的最高价含氧酸的化学式为:HBO4
8.X、Y、Z、W为四种短周期主族元素,其中X、Z同主族,W与X、Y既不同主族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正化合价与最低负化合价的代数和为6。下列说法不正确的是
A.Y、Z两元素的离子的还原性强弱为:Y<Z
B.原子半径由小到大的顺序为:W<X<Z<Y
C.X与W可以形成W2X、W2X2两种化合物
D.相同条件下,Y、Z两元素的最高价氧化物对应水化物的酸性强弱为:Y>Z
|
|
||
|
C |
A |
|
|
|
|
B |
D |
|
7.根据元素周期表和元素周期律的有关知识,下列叙述正确的是
A. 碱金属从锂到铯与水反应的剧烈程度逐渐减弱
B. 卤族元素的单质与氢气反应都需要加热或光照条件
C. 碱金属的活泼性(从锂到铯)依次增强,卤族元素单质(从F2到I2)的活泼性却相反
D. VIA元素的非金属性比VIIA弱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com