
题目列表(包括答案和解析)
6. 下列有关化学用语的说法中不正确的是( )
下列有关化学用语的说法中不正确的是( )
 A.-OH与 都表示羟基 B.次氯酸的结构式为:H-Cl-O
A.-OH与 都表示羟基 B.次氯酸的结构式为:H-Cl-O

C.CH4分子的球棍模型: D.苯分子的比例模型:
5.A和B均为短周期元素,它们的离子A- 和B2+具有相同的核外电子层结构。下面说法正确的是( )
A.原子序数为A > B B.核外电子数为A > B
C. 原子半径A > B D.离子半径 A- > B2+
4.与Ne的核外电子排布相同的阴离子跟与Ar的核外电子排布相同的阳离子所形成的化合物是( )
A.MgBr2 B.Na2S C.CaF2 D.KCl
3. 3月29日,环境保护部(国家核安全局)有关负责人就环境辐射监测情况回答了记者关心的问题。这位负责人介绍说,在安徽省、广东省、广西壮族自治区和宁夏回族自治区的监测点气溶胶取样中除检测到了极微量的人工放射性核素碘-131外,还检测到了极微量的人工放射性核素铯-137和铯-134。已知铯是钠的同族元素,关于铯的下列判断中错误的是 ( )
A.它的金属性比钠强 B.它的最外层电子数为1
C.它有7个电子层 D.单质铯的还原性比单质钠强.
2.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
A.SO2和SiO2 B.CO2和H2
C.NaCl和HCl D.CCl4和KCl
1.《读卖新闻》3月25日:日本东京电力公司24日宣布,在对福岛第一核电站排水口的海水进行取样化验后,检测出含有微量的放射性物质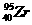 。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于
。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于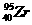 的说法正确的是 (
)
的说法正确的是 (
)
A.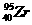 属于非金属元素
属于非金属元素
B.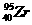 的中子数和电子数之差为55
的中子数和电子数之差为55
C.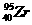 和
和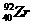 是同种核素
是同种核素
D.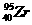 和
和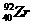 两原子的核外电子总数相等
两原子的核外电子总数相等
28、(9分)将等物质的量A、B气体,置于容积为2L的密闭容器中发生反应,当反应进行到8s末,达到该反应的限度,测得A的物质的量减少0.6mol,B的物质的量减少0.2mol,C的物质的量增加0.4mol,此时n(A):n(B):n(C)=1:2:1。
则:
(1)该反应的化学方程式为: ;
(2)用生成物C表示的该反应的速率为: ;
(3)反应前A、B的物质的量浓度是: 。
2010-2011学年度下学期期中考试
27、(12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
|
实 验 步 骤 |
现 象 |
结 论 |
|
①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 |
反应快慢: Mg>Fe>Cu |
反应物的性质越活泼,反应速率越快。 |
(1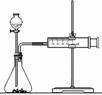 )该同学的实验目的是________________________________;
)该同学的实验目的是________________________________;
要得出正确的实验结论,还需控制的实验条件是________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图
装置进行定量实验。完成该实验应选用的实验药品是______;
应该测定的实验数据是____________________________。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是__________________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是____
A、硫酸钾 B、硫酸锰 C、氯化锰 D、水
26、 (8分)
(8分)
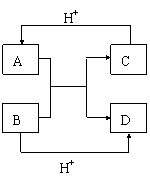
(1)已知A、B、C、D是中学化学中常见的四种不同
 微粒,它们之间存在如图所示的转化关系.如果A、B是
微粒,它们之间存在如图所示的转化关系.如果A、B是
 10电子离子,C、D是10电子分子,A、B、C、D均含有
10电子离子,C、D是10电子分子,A、B、C、D均含有
 两种元素.请写出A、B、C、D四种不同微粒的化学式:
两种元素.请写出A、B、C、D四种不同微粒的化学式:
 A
、B
、
A
、B
、
 C
、D
.
C
、D
.
(2)现有如下两个反应:(A)NaOH + HCl = NaCl + H2O
(B)Zn + CuCl2 = ZnCl2+ Cu
①根据两反应本质,判断能否设计成原电池(A) (B)
②如果能,实验结束后,称得两极质量差为12.9g,则转移电子的物质的量为__________.
③如果不能,说明其原因
25、 (9分)下表为元素周期表的一部分,请回答有关问题:
|
|
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
|
③ |
④ |
⑤ |
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)表中最活泼的金属是______,非金属性最强的元素是______;(填写元素符号)
(2) 最高价氧化物对应水化物酸性最强的化合物是__________;(填写分子化学式)
(3)表中能形成两性氢氧化物的元素是_______,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的离子反应方程式:__________________________________,
___________________________;
(4)比较⑦、⑩单质氧化性的强弱:__________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com