
题目列表(包括答案和解析)
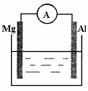
22.(4分)有一定质量的某金属,其原子核内共有3.5×6.02×1023个中子,同质量的该金属和足量的稀硫酸反应共有0.2 mol电子发生转移,生成6.02×1022个阳离子,这些阳离子共有2.8×6.02×1023个电子,则:
(1)该金属摩尔质量为 ;
 (2)原子核内有______个质子,
个中子,其核组成符号为
。
(2)原子核内有______个质子,
个中子,其核组成符号为
。
21.(5分)铍和铝、锂和镁等在元素周期表中具有特殊的“对角线关系”,单质及化合物的性质十分相似。请按要求回答下列各问:
(1)写出Be与NaOH溶液反应的离子方程式(生成Na2BeO2): ;(2)Be(OH)2与Mg(OH)2可用试剂 鉴别,其离子方程式为: ;
20.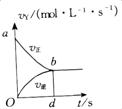 在某2 L容积固定的密闭容器中,充入X、Y两种物质各2 mol,有如下反应:3X(g)+Y(g)
在某2 L容积固定的密闭容器中,充入X、Y两种物质各2 mol,有如下反应:3X(g)+Y(g) 2Z(g)发生,当反应达到平衡后,以Y的物质的量浓度改变表示的反应速率v正和 v逆与时间t的关系如图。则Y的平衡物质的量浓度的表达式(S指对应区域的面积)可表示为( )
2Z(g)发生,当反应达到平衡后,以Y的物质的量浓度改变表示的反应速率v正和 v逆与时间t的关系如图。则Y的平衡物质的量浓度的表达式(S指对应区域的面积)可表示为( )
A、2-Sa O b B、2-Sa b d C、1-Sa O b D、1-Sb O d
第II卷 非选择题(共50分)
19.电子表和电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为一定浓度的KOH溶液,放电时锌极上的电极反应式为:Zn-2e-+2OH-==Zn(OH)2;氧化银电极上的反应式为:Ag2O+2e-+H2O==2Ag+2OH-,总反应式为:Ag2O+H2O+Zn==Zn(OH)2+2Ag。下列说法正确的是( )
A、锌是负极,氧化银是正极
B、锌发生还原反应,氧化银发生氧化反应
C、溶液中OH-向正极移动,K+、H+向负极移动
D、随着电极反应的不断进行,电解质的物质的量保持不变
18.已知1gH2完全燃烧生成水蒸气放出热量121kJ,且O2中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ,则H2中,1molH-H键断裂时吸收热量为( )
A、188 kJ B、436 kJ C、557 kJ D、920kJ
17.已知A、B、C、D的原子序数都不超过18,它们的离子a A( n+1)+、b Bn+、c C( n+1)-、d Dn-均具有相同的电子层结构,则下列叙述正确的是( )
A、原子序数:a>b>c>d
B、离子半径:A(n+1)+>Bn+>C(n+1)->Dn-
C、单质还原性:B>A,单质氧化性:D>C
D、离子还原性:C(n+1)->Dn-,离子氧化性:Bn+>A(n+1)+
16.已知:短周期元素A和B可组成化合物AB3,当A的原子序数为a时,B的原子序数可能是( )①a+4 ②a-4 ③a-8 ④a+2 ⑤a-6 ⑥a+12
A、①②③ B、①④⑤⑥
C、①②③④⑤ D、①②③④⑤⑥
15.一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0% ,与反应前的体积相比,反应后体积缩小的百分率是( )
A、16.7% B、20.0% C、80.0% D、83.3%
14.2011年3月26日,在我省东北部空气中发现了极微量的人工放射性核素碘-131(13153I),初步确认系来自日本核电站事故放射性物质的释放,但这些极微量的放射性物质对我国环境和公众健康不会产生影响,随后东部沿海地区也有类似发现。下列有关说法正确的是( )
A、碘-131是元素碘的一种同位素,正常情况下自然界是不会存在
B、碘-131的化学性质与元素碘不同
C、碘-131的原子核内有74个中子
D、碘元素的相对原子质量是按照包括碘-131在内各种核素原子所占的一定百分比算出的平均值
13.溴化碘(IBr)等卤素互化物的化学性质很像卤素的单质,能与大多数金属、非金属化合生成卤化物,如IBr能与水发生以下反应:IBr+H2O == HBr+HIO,下列有关IBr的叙述中,不正确的是( )
A、在很多化学反应中,IBr是强氧化剂
B、IBr与Zn反应中,ZnI2既是氧化产物,又是还原产物
C、IBr与水反应时既做氧化剂,又做还原剂
D、IBr与AgNO3溶液反应会生成AgBr沉淀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com