
题目列表(包括答案和解析)
25.(14分)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应
3A(g)+B(g) xC(g)+2D(g),经过4min后达到平衡,测得D的浓度为0.5 mol/L
xC(g)+2D(g),经过4min后达到平衡,测得D的浓度为0.5 mol/L
c(A):c(B)=3:5,C的反应速率是0.125 mol·L-1·min-1。
求:(1)A在4 min末的浓度是__________, x的值是__________。
(2)反应前后的压强比为?
24.(14分)看右上图回答下列问题
(1)若烧杯中溶液为稀硫酸,则观察到的现象是 ,电流表指针 (填偏转或不偏转),
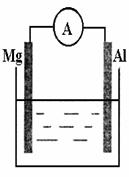 两极反应式为:
两极反应式为:
正极 ;
负极 。
(2)若烧杯中溶液为氢氧化钠溶液,
则负极为 (填Mg或Al),总反应方程式为
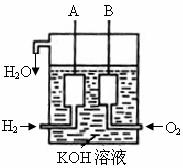
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右下图所
示:A、B两个电极均由多孔的碳块组成。
该电池的正极反应式为: 。
(4)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电
池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,
则该电池的负极反应式为: 。
23、(8分)已知A、B、C、D、E为五种短周期元素构成的离子,A、B、C、D含有10e-,E为双核18e-离子,回答以下问题:
(1)A与B形成的离子化合物甲中既有离子键又有共价键,A与C结合成的化合物乙难溶于水,乙溶于甲的水溶液得无色透明溶液,则C离子的结构示意图为 ,该反应的离子方程式为 。
(2)任何水溶液中都含有A、D两种离子,D离子的电子式为 。
(3)B与E形成的化合物丙,其中离子数之比为2:1,A与D结合成化合物丁,丁与丙反应产生无色无味气体,写出丁的电子式 ,该反应的化学方程式为: 。
(4)有一种液态氮氢化合物戊,是“神舟七号”飞船发射时使用的高能燃料之一,该化合物与E的电子数相同,结构分析得到该分子中只含有单键,则戊的电子式为 。
22.(10分)几种短周期元素的原子半径及某些化合价见下表:
|
元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
|
化合价 |
–1 |
–2 |
+4、–4 |
+6、–2 |
+5、–3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.102 |
0.110 |
0.143 |
0.160 |
0.186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题。涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于 周期, 族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)A与J所形成化合物中的化学键类型是 ,用电子式表示其形成过程 。
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为 。
21.(8分)在N2与H2生成NH3的反应中:拆开1 mol H-H键,1 mol N-H键,1 mol N≡N键分别需要吸收的能量为436 kJ,391 kJ,946 kJ。则理论上1 mol N2参与反应生成NH3___________热量(填:“吸收”或“放出”) ___ ____kJ;1 mol H2参与反应生成NH3___________热量(填:“吸收”或“放出”) _______kJ;事实上,反应的热量总小于理论值,理由是_______________________________________________。
20.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
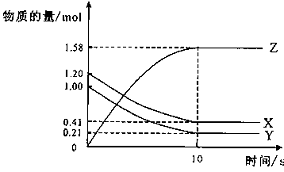
下列描述正确的是
A、反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B、反应开始到10s,X的物质的量浓度减少了0.79mol/L
C、反应开始到10s时,Y的转化率为79.0%
D、反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
第Ⅱ卷(非选择题 共48分)
19.氢气可以在氧气中燃烧,在反应中,断裂1molH2中的化学键消耗的能量为Q1KJ,断裂1molO2中的化学键消耗的能量为Q2KJ,形成1mol H2O中的共价键释放的能量为Q3KJ。下列关系式中,正确的是
A.2Q1+Q2 >Q3 B.Q1+Q2 >2Q3 C.2Q1+Q2 <4Q3 D.2Q1+Q2 <2Q3
18. 近来, 科学家研制了一种新型的乙醇电池(DEFC), 它用磺酸类质子作溶剂, 在200℃左右时供电, 乙醇电池比甲醇电池效率高出32倍且更加安全。电池总反应式为: C2H5OH+3O2
 2CO2+3H2O。下列说法不正确的是
2CO2+3H2O。下列说法不正确的是
A. C2H5OH在电池的负极上参加反应 B. 1 mol乙醇被氧化转移6 mol电子
C. 在外电路中电子由负极沿导线流向正极 D. 电池正极得电子的物质是O2
17.下列关于化学键的说法正确的是
A.构成单质分子的微粒一定含有共价键 B.全部由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子中 D.两种元素组成的分子中一定只有极性键
16. 一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+3B(g) 2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是
一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+3B(g) 2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是
A.C物质的生成速率和分解速率相等 B.容器内气体的密度不再随时间而改变
C.单位时间内生成amol物质A,同时生成3amol物质B D.A、B、C物质的分子数之比为1:3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com