
题目列表(包括答案和解析)
25、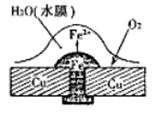 (11分)(1)若2.6g乙炔(C2H2气态)完全燃烧生成液态水和CO2时放热130kJ。则此反应的热化学方程式为:
。
(11分)(1)若2.6g乙炔(C2H2气态)完全燃烧生成液态水和CO2时放热130kJ。则此反应的热化学方程式为:
。
(2) 图中铜板上铁铆钉处容易生锈,被腐蚀的金属是 ,
负极的电极反应式为
 (3)氢气被公认为21世纪替代矿物燃料的理想能源,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则1mol氢气燃烧放出的热量
(3)氢气被公认为21世纪替代矿物燃料的理想能源,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则1mol氢气燃烧放出的热量
是 kJ
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,
请回答:
①氢氧燃料电池的能量转化主要形式是 ,
在导线中电子流动方向为 (用a、b表示)。
②负极反应式为 。
24.普通干电池的电极分别为碳棒和锌筒,以糊状NH4Cl和ZnCl2作电解质(其中
加入 MnO2吸收H2,ZnCl2吸收NH3),电极反应可简化为:Zn-2e-=Zn2+,
2NH4++2e-= 2NH3+H2。根据以上所述判断下列结论不正确的是
A.工作时Zn为负极,发生还原反应
B.工作时电流由碳极经外电路流向Zn极
C.输出电流时碳棒上发生还原反应
D.长时间使用后内装糊状物可能流出,腐蚀用电器
第Ⅱ卷(非选择题 共52分)
23.右图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断

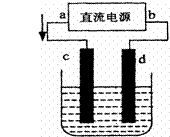 正确的是
正确的是
A.a为负极、b为正极
B.a为阳极、b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
22.从手册上查得:H-H、Cl-Cl和 H-Cl的键能分别为436、243和431 kJ·mol-1,请用此数据估计,下列热化学方程式正确的是
A . H2(g)+Cl2(g)=2HCl(g); △H=-183 kJ·mol-1
B . H2(g)+Cl2(g)=2HCl(g); △H=+183kJ·mol-1
C . H2(g)+Cl2(g)=2HCl(g);△H=-91.5kJ·mol-1
D . H2(g)+Cl2(g)=2HCl(g);△H=+91.5kJ·mol-1
21、根据下表信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
|
主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
20. 根据右图提供的信息,下列所得结论正确的是
根据右图提供的信息,下列所得结论正确的是
A.该反应是吸热反应
B.该反应的生成物比反应物稳定
C.该反应一定可以设计成为原电池
D.该反应向外界放出的热量为E2-E3
19、下列叙述正确的是:
A.P4和CO2均由共价化合物分子构成
B.CCl4和NH4Cl中均存在共价键
C.Na2O和C60晶体中都不存在单个小分子
D.CH4分子是平面型分子,NH3分子的空间构型为三角锥形
18、运用元素周期律来判断,则下列叙述中不正确的是
A.元素Be的金属性比Na的金属性弱
B.At是第6周期第ⅦA族元素,HAt不稳定,且AgAt是有色难溶于水的物质
C.Sr是第5周期第ⅡA族元素,则SrSO4可能难溶于水,Sr(OH)2为强碱
D.As是第4周期第ⅤA 族元素,则AsH3比NH3更稳定
17.可逆反应:2A(g) + 3B(g) 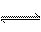 3C(g),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是
3C(g),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是
A.各物质的浓度之比为c(A):c(B): c(C) = 2:3:3
B.A、B、C三者共存
C.混合气体的总质量不变
D.单位时间内, 若消耗了 a mol A 物质, 同时也消耗了 1.5 a mol 的C物质
16.用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.增加Fe的质量
C.滴加几滴CuSO4溶液 D.不用铁片,改用铁粉
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com