
题目列表(包括答案和解析)
4.在实验室中制取纯净、干燥的氯气,常使生成的氯气通过两个洗气瓶,第一个洗气瓶中盛有
( )
A.浓硫酸 B.烧碱溶液
C.饱和食盐水 D.石灰水
[答案]C
[解析]实验室制出的氯气中常混有少量HCl气体和水蒸气,只有先通过盛有饱和食盐水的洗气瓶除去HCl气体后,再除去水蒸气。如顺序颠倒,则干燥后的氯气通过食盐水时又会带出水蒸气,最终不能得到干燥的氯气。
3.下列叙述中能证明次氯酸是一种弱酸的是
( )
A.次氯酸见光分解
B.次氯酸漂白有色布条
C.次氯酸有强氧化性
D.次氯酸钙溶液中通入CO2生成碳酸钙和次氯酸
[答案]D
[解析]用较弱酸与次氯酸盐反应而生成次氯酸,说明HClO为弱酸,HClO见光分解说明其不稳定,漂白有色布条说明其有强氧化性,与酸性强弱无关。
2.检验氯化氢气体中是否混有Cl2,可采用的方法是
( )
A.用干燥的蓝色石蕊试纸
B.用干燥有色布条
C.将气体通入硝酸银溶液
D.用湿润的淀粉碘化钾试纸
[答案]D
[解析]HClO具有漂白性,而Cl2不具有,在干燥环境下,Cl2不能转变为HClO,因而无漂白性,无法与HCl气体区分。两种气体通入AgNO3溶液都产生白色沉淀,因为Cl2与H2O反应也产生Cl-。Cl2与KI反应产生I2,I2遇淀粉变蓝,可以与HCl区分。
1.下列说法正确的是
( )
A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味
B.用排水集气法便可以收集到氯气
C.氯气有漂白性
D.自来水常用氯气来杀菌、消毒
[答案]D
4.2.1活泼的黄绿色气体--氯气
17.为了将混有硫酸钠的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:

(1)操作①能否用硝酸钡溶液?说明理由__________________。
(2)进行操作①后,如何判断SO已除尽,方法是_____________ ________________。
(3)操作②的目的是__________________,为什么不先过滤而后加碳酸钠溶液,其理由是__________________________。
[答案](1)不能,会引入新的杂质(NO)
(2)取少量上层澄清溶液,滴加BaCl2溶液,如无沉淀出现,说明SO除尽
(3)除去过量的Ba2+ 一次性过滤出BaSO4和BaCO3沉淀
16.松花蛋于明朝初年问世,其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl)。将一定比例的配料用水和黏土调制成糊状,敷于蛋上,密封保存,数日后即可食用。
(1)腌制松花蛋的配料用水调制时,发生的主要反应的化学方程式有(不考虑黏土中物质可能参与的反应)_______________________________________________________。
(2)松花蛋外的糊状物经水溶解、过滤后,滤液中肯定大量含有的溶质为______________和______________,可能含有的物质为Ca(OH)2或Na2CO3。
(3)某同学设计如下表所示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
|
实验步骤 |
实验现象 |
结论 |
|
①取少量滤液,滴 加适量K2CO3溶液 |
若出现白色沉淀 |
滤液中含Ca(OH)2 |
|
若无白色沉淀 |
滤液中无Ca(OH)2 |
|
|
②取少量滤液, ____________ |
若出现______ |
滤液中含Na2CO3 |
问题讨论:在什么情况下可以不必做实验②就可以得出结论?
__________________________________________。
[答案](1)CaO+H2O===Ca(OH)2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
(2)NaOH NaCl
(3)滴入适量盐酸 气泡[或滴入Ba(OH)2、BaCl2、CaCl2等溶液 白色沉淀] 若实验①检验出有Ca(OH)2,则肯定没有Na2CO3存在
15.(1)分离沸点不同但又互溶的液体混合物,常用什么方法?________________。
(2)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
__________________________________________________________。
[答案](1)蒸馏法(分馏法)
(2)取一支小试管,打开分液漏斗的活塞,慢慢放出少量液体,往其中加入少量水,如果加水后,试管中的液体不分层,说明分液漏斗中,下层是“水层”,反之,则上层是水层。
[解析]分离沸点不同且互溶的液体混合物通常可以采用的方法是蒸馏(或分馏);证明哪层物质为水,可以将其中的液体取出少量,然后向其中加水,也可以利用水的化学性质进行分析等。
14.请简要叙述下图所示的实验装置、方法、操作中存在的错误。
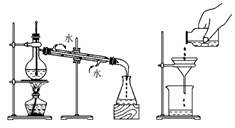
(1)蒸馏乙醇溶液 (2)过滤
[答案](1)温度计下端水银球位置错误;(2)标签向下会被腐蚀,未用玻璃棒引流,漏斗下端未紧靠烧杯内壁
13.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解法 C.结晶法
D.分液法 E.蒸馏法 F.过滤法
(1)分离饱和食盐水与沙子的混合物__________。
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾__________。
(3)分离水和汽油的混合物__________。
(4)分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物__________。
(5)从碘的水溶液里提取碘__________。
[答案](1)F (2)C (3)D (4)E (5)A
[解析]在固体的混合物中,若杂质受热时易分解,可用加热分解法除杂。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com