
题目列表(包括答案和解析)
14.已知反应:
①SO3+H2O===H2SO4 ②Cl2+H2O===HCl+HClO ③2F2+2H2O===4HF+O2 ④2Na+2H2O===2NaOH+H2↑ ⑤2Na2O2+2H2O===4NaOH+O2↑ ⑥SiO2+2NaOH===Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有______________(填序号,下同)。H2O被氧化的是______________,H2O被还原的是__________。属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是__________。
(2)写出反应②的离子方程式:__________。
[答案](1)①⑥ ③ ④ ②⑤
(2)Cl2+H2O===H++Cl-+HClO
[解析]①⑥中元素化合价没有变化,为非氧化还原反应;②中只有氯元素的化合价改变,H2O中元素化合价没有改变,故水既不是氧化剂又不是还原剂;③中氧的化合价从-2价升高为0价,故水被氧化;④中氢元素化合价从+1价降低为0价,故水被还原。⑤H2O中氢氧元素化合价前后未变,故水既不是氧化剂也不是还原剂。
13.已知:Fe2O3+3CO2Fe+3CO2。
(1)标出该反应中电子转移的方向和数目。
(2)指出该反应中,氧化剂是__________,还原剂是__________。
(3)在该反应中,若有2 mol电子发生转移,在标准状况下,可生成CO2的体积为__________。
[答案]

(2)Fe2O3 CO (3)22.4L
[解析]该反应中,Fe元素化合价由+3价降低到0价,被还原,Fe2O3做氧化剂;C元素化合价由+2价升高至+4价,被氧化,CO做还原剂,整个过程,遵循化合价升高的总数=化合价降低的总数=得电子总数=失电子总数,因为OO2,故当2 mol e-发生转移,生成n(CO2)=1 mol,V(CO2)=22.4L。
12.已知KH和H2O反应生成H2和KOH,反应中1 mol KH
( )
A.失去1 mol电子 B.得到1 mol电子
C.失去2 mol 电子 D.没有电子得失
[答案]A
11.(2010年名校联考)氯气是一种重要的工业原料且HCl遇NH3会产生NH4Cl,NH4Cl为白色固体。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是
( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1 mol N2有6 mol电子转移
[答案]C
10.下列表示反应中电子转移的方向和数目正确的是
( )

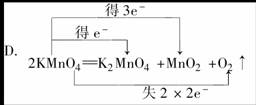
[答案]D
[解析]A中电子数目不正确,应该分别为2×e-;B中得到、失去电子颠倒了;C中箭桥对应错误,应该为:

此处需注意归中反应价态不交叉。
9.氧化还原反应发生在同种元素之间的是
( )
A.Zn+2HCl===ZnCl2+H2↑
B.2H2S+SO2===3S↓+2H2O
C.H2+CuOCu+H2O
D.2H2O2H2↑+O2↑
[答案]B
[解析]A中锌被氧化,H+为氧化剂;B中-2价的硫被氧化,+4价的硫被还原;C中氢气被还原,+2价的铜被还原;D中+1价的氢被还原,-2价的氧被氧化。
8.下列反应既是氧化还原反应又是离子反应的是
( )
A.钠在氯气中燃烧
B.二氧化碳通入澄清的石灰水中
C.氯化钠溶液中滴加硝酸银溶液
D.锌粒放入稀硫酸中
[答案]D
[解析]Na在氯气中燃烧是氧化还原反应但不是离子反应。CO2与澄清的石灰水反应是离子反应但不是氧化还原反应。氯化钠和硝酸银溶液的反应是离子反应但不是氧化还原反应。
7.下列说法中完全正确的是
( )
A.有氧元素参加的反应一定是氧化还原反应
B.没有氧元素参加的反应肯定不是氧化还原反应
C.有单质生成的分解反应一定是氧化还原反应
D.复分解反应一定是氧化还原反应
[答案]C
[解析]有无氧元素参加反应不是判断氧化还原反应的依据,氧化还原反应判断的方法是看元素化合价在反应前后是否有升降。
6.下列叙述中正确的是
( )
A.含氧酸起氧化作用,无氧酸则不能
B.还原剂在反应中得电子
C.还原剂在反应中发生氧化反应
D.氧化剂在同一反应中既可以是反应物,也可以是生成物
[答案]C
[解析]无氧酸中H+也可以发生反应产生H2,有氧化作用。氧化剂只能是反应物,生成物为氧化产物或还原产物。
5.下列说法中正确的是
( )
A.金属单质在反应中只能作还原剂,非金属单质只能作氧化剂
B.某元素从化合态到游离态,该元素一定被还原
C.失电子多的金属还原性强
D.金属阳离子被还原不一定得到金属单质
[答案]D
[解析]金属单质在反应中只能作还原剂,正确,因为金属只能升价,无负价;而非金属单质在反应中既可能作氧化剂,又可能作还原剂,因为大多数非金属既有正价又有负价,故A错误。失电子越容易,物质的还原性越强,与失电子的多少无关,故C错误。元素从化合态到游离态,该元素不一定被还原,如KCl3→2,氧元素被氧化,从CSO4→C,铜元素被还原,故B错。金属元素有些有多种价态,Fe有+2、+3价,若Fe3+被还原可能得到Fe2+,故D正确。氧化还原反应的有关概念是通过化合价的变化来判断的,因此描述时一定要搞清化合价的变化情况。此类题还要善于列举一些实例加以帮助分析,使抽象问题具体化。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com