
题目列表(包括答案和解析)
29.(8分)有下列八种物质:①氯化钡、②金刚石、③硫、④钨、⑤氯化钠、⑥钠、⑦二氧化硅、⑧干冰,回答有关这八种物质的问题。
(1)将这八种物质按不同晶体类型分成四组,并用编号填写下表:
|
各组中物质的编号 |
▲ |
▲ |
▲ |
▲ |
|
晶体类型 |
分子晶体 |
原子晶体 |
离子晶体 |
金属晶体 |
(2)其中以共价键相结合,原子彼此间形成空间网状结构的化合物是 ▲ (填编号)。晶体内存在单个分子的单质是 ▲ (填编号)。
(3)其中硬度最大的物质是 ▲ (填编号);熔点最低的物质是 ▲ (填编号)。
28.(6分)有X、Y、Z三种主族元素形成的3种离子X(n+1)+,Y m-,Z m+,已知m > n,X(n+1)+比Z m+多一个电子层,Z与Y同周期,则进行下列推断:
(1)X、Y、Z三种原子的原子半径由大到小的顺序是 ▲ > ▲ > ▲ 。
(2)X(n+1)+、Y m-、Z m+三种离子的半径由大到小的顺序是 ▲ > ▲ > ▲ 。
(3)三种元素最高价氧化物对应水化物碱性依次减弱,酸性依次增强的顺序是
▲ 。
27.(2分)工业生产中常利用电解反应来制取新的物质,填写下表中电解各物质时阳极(和电源正极相连的极)、阴极(和电源负极相连的极)所得产物的化学式。
饱和食盐水 阳极产物是
氯化铜溶液 阴极产物是
26.(8分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
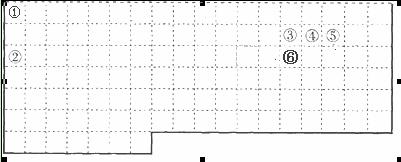
(1)写出①、③两种元素组成的正四面体化合物的电子式 ▲ ,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物的化学式是 ▲ 。
(2)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的产物是 ▲ (写化学式),该物质含有的化学键是 ▲ 。
(3)①和②元素在适当条件下能形成离子化合物,写出该化合物中所含阴、阳离子的结构示意图 ▲ 。
25.(6分)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收249kJ的能量;形成水分子中1 molH-O键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。
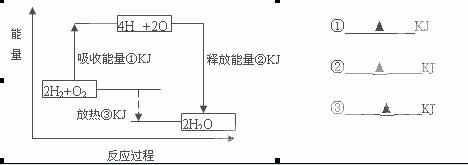
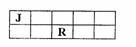
24.J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是
 A.J和氢组成的化合物分子有多种
A.J和氢组成的化合物分子有多种
B.工业上不用电解M和T组成的化合物来制备M
C.R、T两元素的气态氢化物中,R的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
23.以下关于元素周期表的结构叙述正确的是
A.元素周期表有七个主族,八个副族
B.元素周期表有三个长周期(均含18种元素),三个短周期(均含8种元素)
C.第三主族位于元素周期表的第三列(从左往右)
D.零族位于元素周期表的第18列(从左往右)
22.现代城市空气污染物之一NO主要来源于汽车尾气,汽车尾气中产生NO的原因是
A.汽车燃料油(如汽油、柴油)中含氮,NO是其燃烧产物
B.是空气中的N2和汽车燃料油发生了化学反应
C.是汽车排出的高温尾气导致空气中的N2和O2发生化合反应
D.空气中的N2与O2在汽车汽缸内的高温环境下发生反应的产物
21.不能用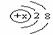 来表示其结构的微粒是
来表示其结构的微粒是
A.Ne B.F- C.Al3+ D.S2-
20.在一密闭容器中进行反应:2SO2(g)+O2(g) 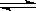 2SO3(g) 测得开始时,SO2、O2、和SO3的浓度分别为0.2mol∙L-1、0.1mol∙L-1、0.2mol∙L-1,在反应过程中不断测该容器中各物质的浓度,下列测定数据肯定不正确的是
2SO3(g) 测得开始时,SO2、O2、和SO3的浓度分别为0.2mol∙L-1、0.1mol∙L-1、0.2mol∙L-1,在反应过程中不断测该容器中各物质的浓度,下列测定数据肯定不正确的是
A.O2为0.15mol∙L-1 B.SO2为0.25mol∙L-1
C.SO3为0.4mol∙L-1 D.O2、SO3的浓度相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com