
题目列表(包括答案和解析)
19. 完成下反应的化学方程式或离子方程式(共6分)
(1)铝与氧化铁在高温下反应(铝热反应)
______________________________________;
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式
____________________________________________________________
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)
____________________________________________________________
18. 针对下面11种元素,完成以下各小题。(共12分)
|
周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
C |
N |
O |
|
Ne |
|
3 |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
|
(1)地壳中含量最多的元素是________(填名称)
(2)化学性质最不活泼的元素是___________(填元素符号)
(3)Al的原子结构示意图为_____________
(4)C与N相比,原子半径较小的是_______(填元素符号)
(5)最高价氧化物对应的水化物碱性最强的是___________(填化学式)
(6)MgO和Al2O3中,属于两性氧化物的是_________________
(7)P、S、Cl的最高价氧化物对应水化物酸性最强的是___________(填化学式)
(8)可用来制造光导纤维的物质是______,晶体硅的主要用途是___________(写出一种)。
⑼ 在S与Cl的单质中,化学性质较活泼的单质是 (填化学式)可用什么化学反应说明该事实(写出反应的化学方程式): 。
17. 按要求填空:(共3分)
(1)M层电子数是L层电子数的一半的元素是 (填元素符号)
(2)最外层电子数是次外层电子数4倍的原子的结构示意图:
(3)用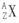 的形式表示,质子数为17,中子数为20的原子:
的形式表示,质子数为17,中子数为20的原子:
16.利用元素周期表的有关知识判断,小明对铍元素(Be)及其化合物的性质的推测不正确的是
A.铍原子的半径小于锂原子的半径;
B.相同条件下,单质铍与酸反应比单质镁与酸反应剧烈;
C.氢氧化铍的碱性比氢氧化钙的碱性弱;
D.单质铍不能与冷水剧烈反应。
15. 下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
A.a原子的最外层电子数比b原子的最外层电子数少
B.常温时,a能从水中置换出氢,而b不能
C.1mol a 从酸中置换出的H2比1 mol b从酸中置换出的H2多
D.a原子电子层数比b原子的电子层数多
14. A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层电子数是最外层电子数的2倍,则A、B元素
A.一定是第2周期元素 B.一定是同一主族元素
C.可能是第2、3周期元素 D.形成化合物一定是离子化合物
13. 已知下列各种元素中A、B两元素的原子序数,其中可形成AB2型共价化合物的是
A. 12和17 B. 6和8 C.12和8 D.11和17
12. X、Y、Z、W为短周期元素,它们在周期表的位置如图所示,若Y原子的最外层电子数是内层电子数的3倍。下列说法中错误的是
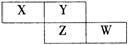 A.X的氢化物的水溶液显碱性
A.X的氢化物的水溶液显碱性
B.Y和Z只能组成一种化合物
C.Z的氧化物和Z的氢化物分别溶于水后,溶液均呈酸性
D.最高价氧化物对应水化物的酸性:W>Z
11.能说明Cl的非金属性比S强的事实有
①常温下S为固体,而Cl2为气体 ②Cl2与H2混合,强光照射剧烈反应;而S与H2反应需较高温度 ③与Fe反应,Cl2生成FeCl3,而S生成FeS ④盐酸是强酸,而氢硫酸是弱酸 ⑤气态氢化物HCl比H2S稳定.
A.①③⑤ B.②③④
C.②③⑤ D.②④⑤
10.具有相同电子层数、原子序数相连的三种元素X、Y、Z,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4,则下列判断正确的是
A.形成的气态氢化物的稳定性:X<Y<Z B. 原子序数: X>Y>Z
C. 原子半径:X>Y>Z D. 得电子能力:X<Y<Z
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com