
题目列表(包括答案和解析)
5、下列说法正确的是
A. 离子化合物中可能含共价键 B. 共价化合物中可能含离子键
C. 离子化合物中只含离子键 D. 共价化合物中一定含离子键
4、已知自然界氧的核素有16O、17O、18O,氢的核素有 H、D,从水分子的原子组成来看,
自然界的水一共有
A. 3种 B. 6种 C. 9种 D. 12种
3、下列电子式,正确的是
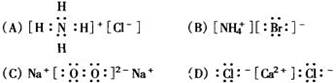
2、元素X的原子有3个电子层,最外层有4个电子。这种元素位于周期表的
A. 第4周期ⅢA族 B. 第4周期ⅦA族
C. 第3周期ⅣB族 D. 第3周期ⅣA族
合题意)
1、据报道,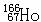 可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为
可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为
A.32 B. 67 C. 99 D.166
22.(14分)已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B ,D 。
(2)画出C元素的离子结构示意图 。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物为 ,
(5)B、C、D三种元素的离子半径由大到小的排列顺序为 (用离子符号表示)。
21、(14分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
b |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
c |
d |
e |
f |
|
|
g |
h |
|
|
|
|
|
|
|
|
|
|
i |
j |
|
k |
l |
m |
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为 。
(2)画出d元 素原子的结构示意图
,其气态氢化物溶于水显
素原子的结构示意图
,其气态氢化物溶于水显  性。(填“酸”或“碱”)
性。(填“酸”或“碱”)
(3)比较 元素g和元素h形成的最高价氧化物的水化物的碱性强弱
>
。
元素g和元素h形成的最高价氧化物的水化物的碱性强弱
>
。
 (4)表中j元素在元素周期表中的位置是
(4)表中j元素在元素周期表中的位置是
 。
。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是
(填写化 合物的化学式,下同),具有两性的是
合物的化学式,下同),具有两性的是  ,
,
20、Ⅰ(4分)用元素符号或化学式回答原子序数11-18的元素的有关问题:
(1)除稀有气体外,原子半径最大的元素是____________ ____;
____;
(2)最高价氧化物对应水化物呈两性的元素是________________;
(3)最高正价氧化物对应水化物酸性最强的酸是________________;
(4)能形成气态氢化物且氢化物最稳定的元素是________________。
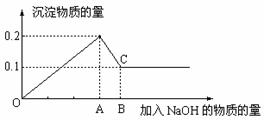
Ⅱ(4分)在MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如下图所示,则溶液中n(Mg2+):n(Al3+)= ,AB段发生的离子反应为
 。
。
19.Ⅰ(4分)(1)写出表示含有8个质子、10个中子的原子的化学符号 。
(2)元素周期表中,所含元素超过18种的周期是  。
。
Ⅱ(6分)有:①168O、178O、188O ②H2O、D2O ③石墨、金刚石 ④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是___________; (2)互为同素异形体的是_______________;
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合物中分子量最大的是_____________(填化学式)。
18.已知 aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
(
)
aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
(
)
A. 原子半径:A>B>C>D
B. 原子 序数:b>a>c>d
序数:b>a>c>d
C. 离子半径:D>C>B>A D. 失电子能力:B>A,得电子能力:D>C 第Ⅱ卷(共46分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com