
题目列表(包括答案和解析)
19.100 mL浓度为2 mol·L-1的盐酸跟过量锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
A.加入适量的6 mol·L-1的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
18.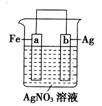
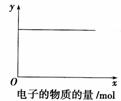 按下图装置实验,若x轴表示流入正极的电子
按下图装置实验,若x轴表示流入正极的电子
的物质的量,则y轴应表示( )
①c(Ag+) ②c(NO3-) ③a棒的质量
④b棒的质量 ⑤溶液的质量
A.①③ B.③④ C.①②④ D.②
17.燃料电池是燃料(如CO、H2、CH4等)跟氧气(或空气)发生反应将化学能转变为电能的装置,若电解质溶液是强碱溶液,下面关于甲烷燃料电池的说法正确的是( )
A.负极反应式:O2+2H2O+4e-===4OH- B.负极反应式:CH4+8OH--8e-===CO2+6H2O
C.随着放电的进行,溶液的pH不变 D.放电时溶液中的阴离子向负极移动
16.有a、b、c、d四种金属。将a与b用导线连接起来,浸入电解质溶液中,外电路电流从b流向a。将a、d分别投入等浓度盐酸中,d比a反应剧烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性由强到弱的顺序是( )
A.dcab B.dabc C.dbac D.badc
15.已知2 mol氢气完全燃烧生成水蒸气时放出热量484 kJ.且氧气中1 mol O==O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中l mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
14.在常温下,把一个盛有一定量的甲烷和氯气的密闭玻璃容器放在光亮的地方,两种气体发生反应,下列叙述中不正确的是( )
A.容器内的原子种类不变 B.容器内的元素种类不变
C.容器内的压强不变 D.发生的反应属于取代反应
13.下列物质中,不可能是乙烯的加成产物的是( )
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
12.下列各物质中,在一定条件下既能发生加成反应,又能发生取代反应,但不能使酸性KMnO4溶液褪色的是( )
A.甲烷 B.苯 C.乙烯 D.乙烷
11.下列各组性质比较的表示中,正确的是( )
A.还原性:HF>HCI>HBr>HI B.稳定性:HF<HCl<HBr<HI
C.与水反应由易到难:Cl2>Br2>I2>F2 D.密度:F2<Cl2<Br2<I2
10.下列关于碱金属性质的叙述中,错误的是( )
A.它们在空气中燃烧都生成R2O(R指碱金属)
B.它们都能与水反应生成氢气和碱
C.所形成的阳离子的氧化性随原子序数递增依次减弱
D.碱金属中密度最小、熔沸点最高的是锂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com