
题目列表(包括答案和解析)
17.某粒子用符号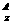 M
M 表示,下列关于该粒子的叙述中,正确的是
表示,下列关于该粒子的叙述中,正确的是
A.所含质子数为(A-n) B.所含中子数为(A-Z-n)
C.所含电子数为(Z+n) D.中子数-电子数=A-2Z+n
16.下列各项所述的两个量,前者一定大于(或高于)后者的是
A.F2和Br2的沸点 B.H-和H+的离子半径
C.同温下分别在100g水中最多能溶解的无水CuSO4的质量和CuSO4·5H2O的质量 D.在NH3+NO → N2+H2O反应中,被氧化和被还原的N原子数
15.去年我国南方发生了半个世纪以来最严重的冰雪灾害。为使道路积雪消融,大量使用了氯化钠、氯化钙等“化冰盐”。下列说法正确的是
A.用“化冰盐”融雪属于化学变化 B.估计MgCl2也可用作“化冰盐”
C.使用“化冰盐”可使水分子结构发生变化
D.大量使用这些“化冰盐”不会造成环境污染
14.下列不能证明氯的非金属性比硫强的实验是
A.HCl比H2S稳定
B.HCl溶液(盐酸)的酸性比H2S溶液(氢硫酸)的酸性强
C.氯水滴入氢硫酸溶液中可出现淡黄色沉淀
D.氯气比硫有更强的氧化性
13.下列各组顺序的排列不正确的是
A.原子半径:Na<Mg<Al B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H4SiO4<H2CO3<CH3COOH D.熔点:金刚石>食盐>干冰
12. 普通锌锰干电池的简图(如右下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:
普通锌锰干电池的简图(如右下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:
Zn+2NH4++2MnO2=[Zn(NH3)2]2++Mn2O3+H2O
关于锌锰干电池的下列说法中正确的是
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池正极的电极反应式为:
2MnO2+2NH4++2e- == Mn2O3+2NH3+H2O
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5g
11.甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时
放出222.5 kJ热量,则表示甲烷燃烧热的热化学方程式为
A. 2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l);ΔH== +890 kJ·mol-1
B. CH4 (g) + 2O2(g) == CO2(g) +2H2O(l);ΔH== +890 kJ·mol-1
C. CH4(g) + 2O2(g) == CO2(g) +2H2O(l);ΔH== -890 kJ·mol-11
D. 2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l);ΔH== -890 kJ·mol-1-1
10.研究下表信息可直接得出的结论是

A.元素性质随原子序数的递增而呈周期性变化
B.同周期元素的非金属性随原子序数递增而增强
C.第VII A族元素的金属性随电子层数增加而减弱
D.第VIIA族元素的非金属性随电子层数的增加而减弱
9.右图装置,电流计指针会偏转,正极变粗,负极变细,符合这种情况的是
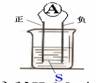 (A)正极:Cu 负极:Zn S: 稀H2SO4
(A)正极:Cu 负极:Zn S: 稀H2SO4
(B)正极:Zn 负极:Cu S: CuSO4溶液
(C)正极:Ag 负极:Zn S: AgNO3溶液
(D)正极:Fe 负极:Cu S: AgNO3溶液
8.下列说法中,正确的是
A.离子化合物中一定不含共价键,共价化合物中一定不含离子键
B.水分子呈直线形,氨分子呈三角锥形
C.碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键
D.分子间作用力越大,分子的热稳定性就越大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com