
题目列表(包括答案和解析)
18.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
A.①③ B.②④ C.①④ D.②③
17.下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
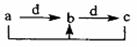
 物质 物质选项 |
a |
b |
c |
d |
|
A |
Al |
Al(OH)3 |
NaAlO2 |
NaOH |
|
B |
N2 |
NO |
NO2 |
O2 |
|
C |
Na2CO3 |
NaHCO3 |
NaOH |
CO2 |
|
D |
Cl2 |
FeCl3 |
FeCl2 |
Fe |
16.右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法不正确的是( )
A.该硫酸试剂的物质的量浓度为18.4mol·L-1
B.该硫酸与等体积的水混合所得溶液的质量分数大于49%
C.配制250mL 4.6mol·L-1的稀硫酸需量取该硫酸62.5mL
D.2.7gAl与足量的该硫酸反应可得到标准状况下的H2 3.36L
15. 某钠盐溶液中可能含有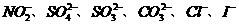 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:①用pH计测得溶液成碱性 ②加入盐酸,产生有色刺激性气体
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:①用pH计测得溶液成碱性 ②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
 ⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色。该同学最终确定在上述六种离子中含
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色。该同学最终确定在上述六种离子中含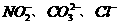 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
14.下列离子方程式表达正确的是
A.用惰性电极电解熔融氯化钠: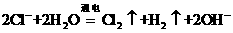
B.用氢氧化钠溶液除去铝表面的氧化膜: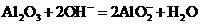
C.用稀氢氧化钠溶液吸收二氧化氮:
D.用食醋除去水瓶中的水垢: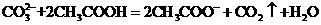
13.从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A.此法的优点之一是原料来源丰富 B.①②③步骤的目的是从海水中获取MgCl2
C.提取镁的过程涉及化合、分解、置换反应D.第④步电解时,还会产生副产品氯气
12.有相同的三块铝片,进行如下实验
实验一:取第一块铝片,直接放入硫酸铜溶液中观察现象
实验二:取第二块铝片,用砂纸擦试表面后,放入硫酸铜溶液中观察现象
实验三:将实验一中铝片从硫酸铜溶液中取出,洗净后放入氢氧化钠溶液中,片刻后取出铝片,洗净后再放入硫酸铜溶液中观察现象
实验四:取第三块铝片,用砂纸擦试表面后,置于浓硝酸中,片刻后取出,洗净,再放入硫酸铜溶液中观察现象。综合以上四个实验的主要目的是试图说明
A.铝片能和硫酸铜溶液反应 B.铝片能和氢氧化钠溶液反应
C.铝片不能和硝酸反应 D.铝片表面能形成具有保护作用的氧化膜
11.已知:H2(g)+F2(g) 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
10.在如图所示的装置中,烧瓶中充满干燥的气体a,将滴管内的液体b挤入烧瓶内,轻轻振荡烧瓶,并打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
|
|
a(干燥气体) |
 b(溶液) b(溶液) |
|
A |
NO2 |
水 |
|
B |
SO2 |
NaHCO3溶液 |
|
C |
NH3 |
稀盐酸 |
|
D |
Cl2 |
饱和NaCl溶液 |
9.设NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA
B.标准状况下,14g氮气含有的核外电子数为5NA
C.足量Zn与一定量的浓硫酸反应,产生标准状况下22.4L气体,转移的电子数为2NA
D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com