
题目列表(包括答案和解析)
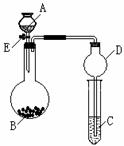
28.(10分)某同学设计了下图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:(20分)
(1)若A为浓氨水,B为烧碱,C中盛有AlCl3溶液,旋开活塞
E,足够长时间后,观察到C中的现象为 ,C中
发生反应的离子方程式为 ;
(2)若A为30%的H2O2溶液,B为二氧化锰,C中盛有酸化过
的FeCl2溶液,旋开活塞E后,C中的现象为 ,
C中发生反应的离子方程式为 ;
(3)利用上述装置还可以验证物质的性质,如设计证明酸性:
H2CO3>H2SiO3,则A中加盐酸,B中加 固体,C中加 溶液,观察到C中的现象是 ;
(4)利用上述装置还可以验证SO2的化学性质, A为硫酸,B为亚硫酸钠,那么C中盛有 溶液可验证其氧化性;C中盛有 溶液可验证其还原性; 而C中盛有 溶液可验证其漂白性。
27.(8分)下图是常见物质间的转化关系,其中部分产物已被略去。常温下X为固体、B为液体,A、C、E为气体,单质M是目前使用量最大的金属。X受热分解生成A、B、C的物质的量相等。回答下列问题:
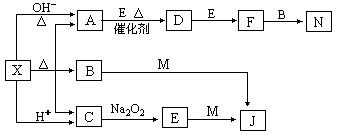
⑴写出X的名称:_____________;C的电子式_____________;
⑵写出A→D反应的化学方程式:______________________________________;
 ⑶写出Mg在C中点燃时化学方程式:________________________________;
⑶写出Mg在C中点燃时化学方程式:________________________________;
⑷写出N的稀溶液与过量M反应的离子方程式:_______________________________________;
26.(4分)下列有关实验操作或判断不正确的是 (填序号,多选扣分)。
A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大。
B.用干燥的pH试纸测定氯水的pH值。
C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌。
D.100 mL容量瓶可用于配制95 mL 0.1 mol/L NaCl溶液。
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量。
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
G.苯、CCl4、酒精可用来萃取溴水中的溴。
H.实验室保存氯化亚铁溶液时,加入少量铁粉。
25、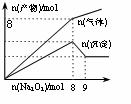 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
A.2 mol、3 mol、8 mol B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol D.3 mol、2 mol、4 mol
24.下列叙述正确的是( )。
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜能加快反应速率。
②锌层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀。
③电镀时,应把镀件置于电镀槽的阴极。
④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解。
⑤钢铁表面常易锈蚀生成Fe2O3·nH2O。
A.①②③④⑤ B.①③④⑤ C.①③⑤ D.②④
23.一定温度下,可逆反应2NO2 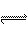 2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:①单位时间内生成n mol
O2的同时生成2n mol NO2;②单位时间内生成n mol
O2的同时生成2n mol NO;③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态;④混合气体的颜色不再改变的状态;⑤密闭容器中压强不再改变的状态;⑥混合气体的平均相对分子质量不再改变的状态。
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:①单位时间内生成n mol
O2的同时生成2n mol NO2;②单位时间内生成n mol
O2的同时生成2n mol NO;③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态;④混合气体的颜色不再改变的状态;⑤密闭容器中压强不再改变的状态;⑥混合气体的平均相对分子质量不再改变的状态。
A.①④⑤⑥ B.②③⑤⑥ C.①③④⑥ D.全部
22.将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:
3A(g)+B(g)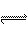 xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol·L-1·min-1,下列说法正确的是
xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol·L-1·min-1,下列说法正确的是
A. 以B表示的平均反应速率为v(B)=0.13 mol·L-1·min-1 B. 4min时,A的物质的量为0.75mol
C. 该反应方程式中,x=3 D. 4min时,A的转化率为50%
21.短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是( )
A.E是一种金属元素 B.在ECln中E与Cl之间形成离子键
C.E的一种氧化物为EO D.E位于元素周期表的ⅡA族
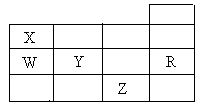
20.右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A.Y、Z的阴离子电子层结构都与R原子的相同
 B.常压下,Y单质的沸点比Z单质的沸点低
B.常压下,Y单质的沸点比Z单质的沸点低
C.W的氢化物的稳定性比X的氢化物的稳定性强
D.Y元素的非金属性比W元素的非金属性强
19.下列说法正确的是
A.原子最外层电子数为2的元素一定处于周期表IIA族
B.主族元素X、Y能形成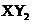 型化合物,则X与Y 的原子序数之差可能为2或5
型化合物,则X与Y 的原子序数之差可能为2或5
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com