
题目列表(包括答案和解析)
23.(9分)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。


(1)T℃时将3mol SO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol
, 则达到平衡时SO2的转化率为 。(1分)
SO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol
, 则达到平衡时SO2的转化率为 。(1分)
(2)下列叙述能证明该反应已达化学平衡状态的是 (填序号)(2分)
①SO2的体积分数不再发生变化 ②容器内压强不再发生变化 ③容器内气体分子总数不再发生变化 ④相同时间内消耗2n molSO2的同时生成n molO2 ⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3) 反应 (填“放出”或“吸收”) 热量(用E1、E2或E3表示)(2分)。
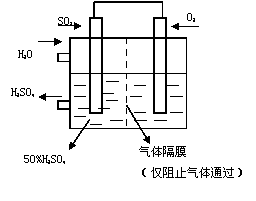 (4)若以右图所示装置,用电化学原理生产硫酸,
(4)若以右图所示装置,用电化学原理生产硫酸,
将SO2、O2以一定压强喷到活性电极上反应。
写出两电极的电极反应式:
;
。(2分) [来网]
为稳定持续生产,硫酸溶液的浓度应维持不变,则通入S O2和水的质量比为 (2分)
O2和水的质量比为 (2分)
22.(7分,每空1分)A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质。试回答:
(1)A、B、C、D的元素符号分别为______、____ 、 、______。
(2)用电子式表示A与C形成化合物的过程:
_________________________________________________。
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
_________________________________ 。
(4)写出实验室制备D的单质的化学反应方程式:
__________________________________________。
21.(3分)按已知的原子结构规律,82号元素X应是第___________周期___________族元素,它的最高正价氧化物的化学式为_____________(该元素的元素符号用X表示)。
20.a mL三种气态烃的混合物和足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),气体体积共缩小2a mL(不考虑二氧化碳的溶解)。则三种烃可能的组合是( )
A.CH4、C2H4、C3H4任意体积比
B.CH4、C3H6、C2H2保持C3H6∶C2H2=1∶ 2(物质的量之比)
C.C2H6、C4H6、C2H2同条件下体积比为2∶1∶1
D.C3H8、C4H8、C2H2质量比为11∶14∶26
第Ⅱ卷 (非选择题,共50分)
19. 某烃的结构简式为
,它可能具有的性质是( )
某烃的结构简式为
,它可能具有的性质是( )
A.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B.它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
C.易溶于水,也易溶于有机溶剂
D.能发生加成反应,一定条件下1mol该有机物最多可与4mol氢气加成
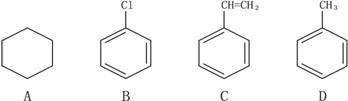
18.下列物质中所有原子都有可能在同一平面上的是( )
17.某化合物的分式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个
-CH- 和一个-Cl,则它的可能结构有几种( )
A.2种 B.3种 C.4种 D.5种
16.利用下列反应制备括号中的物质,不合理的是( )
A.乙烯与氯气加成(1,2-二氯乙烷)
B.乙烯与水加成(乙醇)
C.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
D.氯气与苯用氯化铁做催化剂反应(氯苯)
15.Li-Al/FeS电池是一种正在开发的车载电 池,该电池中
池,该电池中 正极的电极反应式为:
正极的电极反应式为:
2Li+ + FeS + 2e- == Li2S + Fe ,有关该电池的下列叙述中正确的是 ( )
A.该电池的电池反应式为:2Li + FeS == Li2S + Fe
B.Li-Al合金在电池中作为正极材料
C.负极的电极反应式为:Al - 3e- == Al3+
D.Li-Al/FeS电池中,电子经外电路流入Li-Al极
14.
 如下图,先向B中充入2molX、2molY,关闭活塞K,再向A充入1molX、1molY,使起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,两容器中各自发生下述反应,X(g)+ Y(g) 2 Z(g)+W(g
如下图,先向B中充入2molX、2molY,关闭活塞K,再向A充入1molX、1molY,使起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,两容器中各自发生下述反应,X(g)+ Y(g) 2 Z(g)+W(g ); A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L 。下列说法错误的是( )
); A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L 。下列说法错误的是( )
A.反应速率:v(B) >v(A)
>v(A)
B.A容器中X的转化率为 80%
C.A中混合气体密度不再变化能够证明 A中反应达到平衡状态
D.B中混合气体密度不再变化能够证明 B中反应达到平衡状态
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com