
题目列表(包括答案和解析)
26.有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某同学设计了如图装置(夹持装置仪器已省略),其实验操作为:按图安装好,先关闭活塞a、b、c,在铜丝的中间部分加热片刻。然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
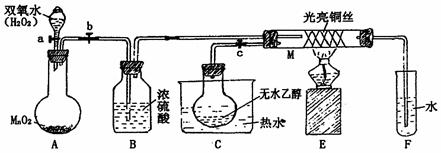
(1) A中发生反应的化学方程式: ,
B的作用: ;C中热水的作用: 。
(2) M处发生反应的化学方程式为: 。
(3) M管中可观察到的现象: ,从中可认识到该实验过程中催化剂 (填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的 。
(4) 验证乙醇氧化产物的试剂是 ,并写出对应的化学方程式 。
(5) 若试管F中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 ,要除去该物质,可先在混合液中加入 (填写字母)。
a、氯化钠溶液 b、苯 c、碳酸氢钠溶液 d、四氯化碳
25.T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示,3分钟时达到平衡;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。
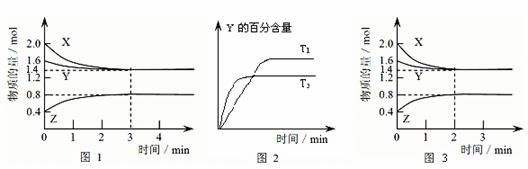
(1)容器中发生的反应可表示为______ ________ ________ __
(2)反应进行的前3 min内,用X表示的反应速率 v(X)=____________mol/(L·min)
(3)保持其他条件不变,升高温度,该反应的化学平衡将向________方向移动(填“正反应”或“逆反应”)
(4)①若改变反应条件,使反应进程如图3所示,则改变的条件是____________
②一定条件下的密闭容器中,该反应达到平衡,要提高气体Y的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.减少Z的浓度 d.增加气体Y的浓度
24.已知常温常压下:① 3Cl2+2NH3→N2+6HCl , ② 3Cl2+8NH3→N2+6NH4Cl
(1)完成并配平反应③的化学方程式,并标出电子转移方向和数目:
③ 3Cl2+4NH3→
(2)在反应③中:还原剂是 ,还原产物是 。
(3)若按③反应后产生气体4.48 L(标准状况),则被氧化的气体的物质的量是 mol。
23.(1)原子核内无中子的元素可放在元素周期表的 族,又根据最高正化合价和负化合价的绝对值相等可放在 族,该元素还可放在元素周期表的 族。它的核外电子排布式为 ,它和氧元素可形成的化合物的电子式为 。
(2)科学家发现在特殊条件下,水能表现出许多有趣的结构和性质。 一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”。

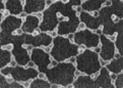
A B
则A、B两幅图中能表示“热冰”的示意图为 。使水结成“热冰”采用“弱电场”的条件,说明水分子是 分子。(选填“极性”或“非极性”)
(3)用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子(H2O+)。这种阳离子具有较强的氧化性,试写出该离子与H2S的水溶液反应的离子方程式 ;该反应破坏的化学键是 。
22.实验室将9g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为l8g,则该氧化物粉末可能是
A.Fe2O3和MnO2 B.MnO2和V2O5 C.Cr2O3和V2O5 D.Fe3O4和FeO
第Ⅱ卷 (共84分)
21.pH与体积都相同的硫酸和醋酸溶液,分别与同物质的量浓度、同体积的Na2CO3溶液反应,若在相同条件下放出CO2的量相同,则下列推断合理的是
A.Na2CO3过量 B.Na2CO3恰好与醋酸完全反应
C.Na2CO3恰好与硫酸完全反应 D.两种酸都过量
20.将0.2mol/L的醋酸钠溶液10mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
A.c(Na+)+c(H+)=c(Ac-)+c(Cl-)+c(OH-) B.c(HAc)>c(Cl-)>c(Ac-)>c(H+)
C.c(Ac-)>c(Cl-)>c(HAc)>c(H+) D.c(Ac-)=c(Cl-)=c(HAc)>c(H+)
19.利用下列装置(部分仪器已省略),能顺利完成对应实验的是
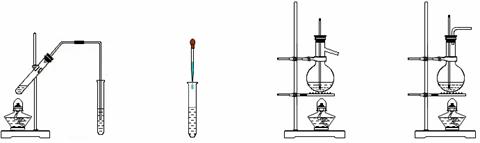
A.制硝基苯 B.制氢氧化亚铁 C.实验室制乙烯 D.石油的蒸馏
18.下列离子方程式,一定正确的是
A.硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S
B.纯碱溶液中滴加少量盐酸:CO32- + H+ → HCO3-
C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O
D.将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO
17.在铁与铜的混和物中,加入一定量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,m1与m2的关系是
A.m1 g固体中一定有铁 B.m1一定大于m2
C.m1可能等于m2 D.m1可能大于m2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com