
题目列表(包括答案和解析)
24.下列事实中能证明氯化氢是共价化合物的是
A.液态氯化氢不导电 B.氯化氢极易溶于水
C.氯化氢不易分解 D.氯化氢溶液可以电离
23.现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
最外层电子数为是次外层电子数的2倍 |
|
X |
L层有三个未成对电子 |
|
Y |
L层p电子数比s电子数多两个 |
|
Z |
元素的最高正价为+7价 |
下列说法正确的是
|
 B.分子TY2的键角为180°
B.分子TY2的键角为180°
C.T元素在周期表中的表示为:
 D.XZ3为非极性分子
D.XZ3为非极性分子
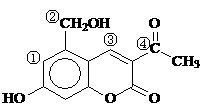
22.针对齐齐哈尔第二 制药有限公司生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如右图。下列关于“亮菌甲素”的说法中,不正确的是
制药有限公司生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如右图。下列关于“亮菌甲素”的说法中,不正确的是
A.亮菌甲素的分子式为C12H9O5
B.分子中所有碳原子可能在同一平面上
C.①②③④处碳原子的杂化类型分别是:sp、sp3、sp2、sp3
D.1 mol亮菌甲素最多能消耗H2和NaOH的物质的量分别为5 mol和3 mol
21、下列说法正确的是( )
A、离子化合物中可能含有共价键
 B、分子晶体中的分子内不含有共价键
B、分子晶体中的分子内不含有共价键
C、分子晶体中一定有非极性共价键
D、分子晶体中分子一定紧密堆积
20、根据对角线规则,下列物质的性质具有相似性的是( )
A、硼和硅 B、铝和铁 C、铜和金 D、铍和铝
19.下列对分子的性质的解释中,不正确的是
A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
 B.乳酸(
B.乳酸( )有一对对映异构体,因为其分子中含有一个手性碳原子
)有一对对映异构体,因为其分子中含有一个手性碳原子
C.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
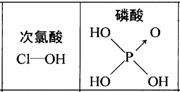
D.由右图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数
18.下列数据是对应物质的熔点,有关的判断正确的是
|
Na2O |
Na |
AlF3 |
AlCl3 |
Al2O3 |
BCl3 |
CO2 |
SiO2 |
|
920℃ |
97.8℃ |
1291℃ |
190℃ |
2073℃ |
-107℃ |
-57℃ |
1723℃ |
A.只要含有金属阳离子的晶体就一定是离子晶体,如AlF3和Al2O3等
B.在共价化合物分子中各原子都形成8电子结构,如BCl3和CO2等
C.同主族元素的氧化物可形成不同类型的晶体,如CO2和SiO2等
D.金属元素与非金属形成的晶体一定是离子晶体,如Na2O、AlF3和AlCl3等
17. 在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是( )
在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是( )
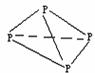
A.石墨的结构 B.白磷的结构
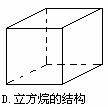
C.CCl4的结构 D.立方烷(C8H8) 的结构

|
16.下列叙述正确的是( )
A.HF、HCl、HBr、HI的熔点沸点依次升高
B.具有相同质子数和电子数的两种粒子,有可能一种是分子,一种是离子
C.稀有气体一般难于发生化学反应,是由于其键能大
D.元素的性质呈现周期性变化的根本原因是元素原子的核外电子排布呈周期性变化
15.下列有关金属的说法正确的是( )
A.金属原子的核外电子在金属晶体中都是自由电子
B.镁型和铜型的原子堆积方式空间利用率最高
C.金属原子在化学变化中失去的电子数越多,其还原性越强
D.金属导电的实质是金属阳离子在外电场作用下的定向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com