
题目列表(包括答案和解析)
25、(8分)某光卤石(KCl·MgCl2·6H2O)样品中含有不跟NaOH溶液、盐酸反应的杂质。某校化学课外活动研究小组现测定此样品中含有KCl·MgCl2·6H2O的质量分数,经讨论有多种实验测定方案。请根据提供的实验试剂和仪器(所需要的仪器任选),选择精确度较高的实验测定方案,简要写出第二步以后的实验步骤和实验结果。
(1)可选用的实验试剂:
①amol/LNaOH溶液②bmol/LNa2CO3溶液③cmol/LHCl溶液④dmol/LAgNO3溶液⑤酚酞溶液⑥紫色石蕊试液
(2)实验步骤:第一步:称取mg样品,放入250mL容量瓶中,加适量水溶解。
 第二步: ;第三步: ;第四步:
。
第二步: ;第三步: ;第四步:
。
(3)计算样品中含有KCl·MgCl2·6H2O(相对分子质量277.5)的在 质量分数表达式: 。(如果用以上试剂,其体积可分别用AmL、BmL、CmL、DmL表示)
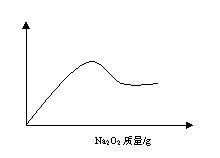
24、(3分)某溶液A可能含有NH4+、Na+、Mg2+、Al3+、Fe3+、CO32-、SO42-等离子中的几种,取部分A溶液,加盐酸酸化后再滴入氯化钡溶液,只出现白色沉淀;另取部分A溶液,加入固体Na2O2有无色、无味的气体产生,并有白色沉淀生成,沉淀的量与所加Na2O2的关系如图所示,据此判断,溶液中一定含有 离子,一定不存在 离子,可能含有 。
23、(4分)甲、乙两瓶溶液,可能是AlCl3和NaOH。向10mL0.2 mol/L甲溶液中滴加未知的乙溶液,测得滴加15mL与45mL时,所得沉淀得质量相等。请回答:
(1)甲溶液为: ,乙溶液为:
(2)滴加45mL乙溶液的过程中发生的离子方程式为: 。
 (3)乙溶液的物质的量浓度为:
。
(3)乙溶液的物质的量浓度为:
。
22、(14分)下列图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。已知:A是固体单质;B、X、H为气体单质;D属于可溶于水的强电解质,一个D分子中含有18个电子。
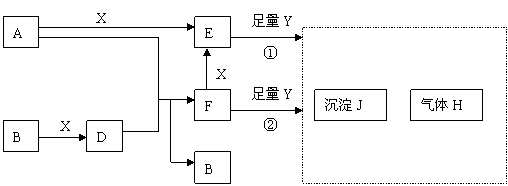

(1)化学式:B为 ,F为 。
(2)用电子式表示D的形成过程为: 。
(3)已知H的密度比空气大,则①中所涉及的反应的化学方程式为:
; 。
(4)写出F与足量Y反应生成J的理由: 。
(5)写出A与D溶液反应生成B的离子方程式: 。
写出A在一定条件下与水反应的化学方程式: 。
21、(3分)某校自产的“××”牌矿泉水,富含锶元素,锶在生物体中是痕量元素(即每日需求量低于0.04g)。根据周期表,请回答下列问题:
(1)请指出锶在元素周期表中的位置: 。(2)氢氧化锶是强碱还是弱碱: 。
(3)请用最简便的方法证明氢氧化锶是强碱还是弱碱: 。
20、某铁的氧化物,用7mol/L的盐酸100mL在一定条件下恰好完全反应,所得溶液中再通入0.56L标准状况下的氯气时,刚好使溶液中Fe2+完全转化为Fe3+,则该氧化物的化学式表示为:
A.FeO B.Fe3O4 C.Fe4O5 D.Fe5O7
19、将 5.1g镁铝合金投入到500mL2mol/LHCl中,金属完全溶解,再加入4mol/LNaOH溶液,若要生成的沉淀最多,则应加入的这种NaOH溶液的体积是:
A.200mL B. 250mL C. 425mL D. 560mL
18、下列的说法不正确的是:
A. PH=7的溶液不一定是中性溶液
B.pH=11的氨水和氢氧化钠加水稀释1000倍,其pH值氨水大于氢氧化钠
C.100℃时,2LpH=8的Ba(OH)2的溶液与9LpH=5的稀硫酸溶液混合, pH近似为7
D. 亚硫酸钠溶液在空气中蒸干得到的固体是Na2SO3
17、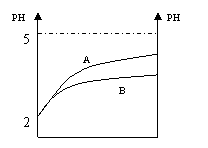 常温下,pH=2的两种溶液HA和HB,分别加水
常温下,pH=2的两种溶液HA和HB,分别加水
稀释1000倍,其pH与所加水的体积变化如图所示,
则下列说法正确的是:
A.酸HB是比酸HA更强的酸
B.酸HA是强酸,HB是弱酸
C.稀释前酸HA的物质的量浓度比HB大
D.稀释前酸HB比HA的物质的量浓度大
16、有二元酸(简写为H2R)溶液,按下式发生电离:

 H2R
H+ +HR- HR- H++R2-
H2R
H+ +HR- HR- H++R2-
设有下列四种溶液:①0.01mol/L 的H2R溶液 ②0.01mol/L 的NaHR溶液③0.02mol/L HCl溶液与0.04mol/LNa2R溶液的等体积混合液 ④0.02mol/L的NaOH溶液和0.02mol/L的NaHR溶液的等体积混合液。下列说法正确的是:
A.c(H+)最大的是① ,最小的是② B.pH值最大的是①最小的是④
C.c(R2-)最大的是④ 最小的是① D.c(HR-)最大的是③最小的是①或④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com