
题目列表(包括答案和解析)
0.105mol·L-1、c(Al3+)=0.055mol·L-1,溶液的pH=2.0(假设溶液中硫酸完全电离
为H+和SO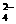 ),则c(K+)为
( )
),则c(K+)为
( )
A.0.045mol·L-1 B.0.035mol·L-1 C.0.055mol·L-1 D.0.040mol·L-1
8、将硫酸钾、硫酸铝、硫酸钾铝三种盐混合溶于硫酸酸化的水中,测得c(SO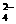 )=
)=
7、下列物质中属于电解质,但在给定条件下不能导电的是 ( )
A.稀硫酸 B.液态溴化氢 C.铝 D.蔗糖
6、把0.05 mol NaOH固体分别加入到100 mL下列液体中,溶液的导电能力变化最小的
是 ( )
A.自来水 B.0.5 mol·L-1盐酸
C.0.5 mol·L-1CH3COOH溶液 D.0.5 mol·L-1KCl溶液
5、向氨水中加入NH4Cl晶体,溶液的碱性 ( )
A.增强 B.减弱 C.不变 D.为零
4、20℃时H2S饱溶液1L,其浓度为0.1mol·L-1,其电离方程式为H2S===H++HS-,HS-===H++S2-,若要使该溶液[H+]及[S2-]都减小,可采取的措施是 ( )
A、加入适量的水 B、加入适量的NaOH固体
C、通入适量的SO2 D、加入适量的CuSO4固体
3、下列叙述中,能证明某物质是弱电解质的是 ( )
A.熔化时不导电 B.不是离子化合物,而是极性共价化合物
C.水溶液的导电能力很差 D.溶液中已电离的离子和未电离的分子共存
2、下列电离方程式中,错误的是 ( )
 A.Al2(SO4)3===2Al3++3SO42- B.HF H++F-
A.Al2(SO4)3===2Al3++3SO42- B.HF H++F-

 C.HI H++I-
D.Ca(OH)2 Ca2++2OH-
C.HI H++I-
D.Ca(OH)2 Ca2++2OH-
1、下列叙述中正确的是 ( )
A.物质的溶解过程,实质上就是其电离过程
B.二氧化硫的水溶液能导电,所以二氧化硫是电解质
C.1 L 0.1 mol·L-1的H2SO4溶液中含有0.2 mol的H+
D.1 L 0.2 mol·L-1的H2SO3溶液中含有0.2 mol的H+
26、(6分)用下面改进的方法可以制得白色的Fe(OH)2沉淀。在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
(1)在试管Ⅰ里加入的试剂是 。(2)在试管Ⅱ里加入的试剂是 。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是 。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是 。
华中师大一附中2005-2006学年度第一学期
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com