
题目列表(包括答案和解析)
8.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
7.将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则
溶液中有关微粒的浓度关系正确的是( )
A.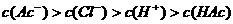
B.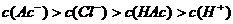
C.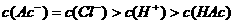
D.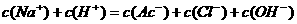
6.在含有酚酞的0.1mol/L氨水中加入少量的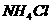 晶体,则溶液颜色( )
晶体,则溶液颜色( )
A.变蓝色 B.变深 C.变浅 D.不变
5.取pH均等于2的盐酸和醋酸各100mL分别稀释2倍后,再分别加入0.03g锌粉,
在相同条件下充分反应,有前叙述正确的是( )
A.醋酸与锌反应放出氢气多 B.盐酸和醋酸分别与锌反应放出氢气一样多
C.醋酸与锌反应速率大 D.盐酸和醋酸分别与锌反应的速率一样大
4.下列物质的水溶液能导电,但属于非电解质的是( )
A.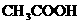 B.
B.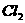 C.
C.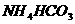 D.
D.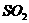
3.水的电离过程为 ,在不同温度下其离子积常数为
,在不同温度下其离子积常数为
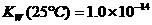 ,
,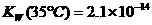 .则下列叙述正确的是( )
.则下列叙述正确的是( )
A.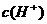 随着温度的升高而降低 B.在35℃时,水中的
随着温度的升高而降低 B.在35℃时,水中的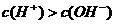
C.水的电离度α(25℃)较大 D.水的电离是吸热的
2.日常生活中人们常喝纯净水,市场上出售的纯净水有一些是蒸馏水.对于这一类纯
净水的下列说法,正确的是( )
A.它能够导电 B.它含有人体所需的矿物质和多种微量元素
C.它的pH=0 D.它清洁、纯净,但长期饮用对健康无益
1.“垃圾是放错了位置的资源”,应该分类回收.生活中废弃的铁锅、铝制易拉罐、
铜导线等可以归为一类并加以回收,它们属于( )
A.氧化物 B.电解质 C.金属或合金 D.非电解质
25.完全燃烧某烃A,并收集产生的全部水蒸气,恢复至室温时,测得水的质量正好等于该烃的质量,按要求回答下列问题:
(1)该烃的最简式是 。
(2)若该烃为气态炔烃,则可能的结构简式为: 、 。
(3)若该烃为液态芳香烃,写该烃中相对分子质量最小的烃的分子式 。
23.(本小题6分)电石中的碳化钙和水能完全反应:
CaC2+2H2O=C2H2↑+Ca(OH)2
 使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
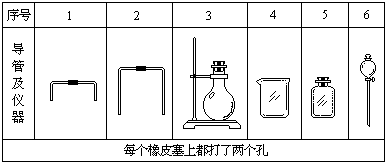
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是( )接( )接( )接( )接( )接( )。(2分)
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。.
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。(2分)
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含
有 杂质。(1分)
(4)若实验时称取的电石1.60克,测量排出水的体积后,折算成标准状况乙炔的体积为448毫升,此电石中碳化钙的百分含量是 %。(1分)
|
|
季碳原子,数目分别用n1、n2、n3、n4表示。例如 分子中n1=6,
n2=1,n3=2,n4=1。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子个数为n0。n0与n1、n2、n3、n4的关系是:n0= 或
n0= 。
(2)四种碳原子数之间的关系为n1= 。
(3)若某分子中 n2=n3=n4=1,则该分子的结构简式可能是(写其中一种) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com