
题目列表(包括答案和解析)
6. 分子为C4H9Cl的同分异构体有
A. 1种 B. 2种 C. 3种 D. 4种
5. 相同温度下等物质的量浓度的下列溶液中,pH值最小的是
A.
NH4Cl
B. NH4HCO3 C. NH4HSO4 D. 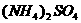
4. 将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
A. 稀硝酸 B. 稀盐酸 C. 硝酸铜 D. 氢氧化钠
3. 以NA表示阿佛加德罗常数,下列说法中正确的是
A. 53g碳酸钠中含NA个CO32-
B. 0.1molOH-含NA个电子
C. 1.8g重水(D2O)中含NA个中子
D. 标准状况下11.2L臭氧中含NA个氧原子
2. 下列物质中不会因见光而分解的是
A. NaHCO3 B. HNO3 C. AgI D. HClO
1. 下列物质中属于离子化合物的是
A. 苛性钾 B. 碘化氢 C. 硫酸 D. 醋酸
低价态的还原性:
4Fe(OH)2+O2+2H2O===4Fe(OH)3
与酸性物质的作用:
2NaOH+SO2(少量)===Na2SO3+H2O NaOH+SO2(足量)===NaHSO3
2NaOH+SiO2===NaSiO3+H2O 2NaOH+Al2O3===2NaAlO2+H2O
2NaOH+Cl2===NaCl+NaClO+H2O NaOH+HCl===NaCl+H2O
NaOH+H2S(足量)===NaHS+H2O 2NaOH+H2S(少量)===Na2S+2H2O
3NaOH+AlCl3===Al(OH)3↓+3NaCl NaOH+Al(OH)3===NaAlO2+2H2O
NaOH+NH4Cl===NaCl+NH3↑+H2O Al(OH)3+NH4Cl 不溶解
3,不稳定性:
Mg(OH)2===MgO+H2O 2Al(OH)3===Al2O3+3H2O
2Fe(OH)3===Fe2O3+3H2O Cu(OH)2===CuO+H2O
八,盐
1,氧化性:
2FeCl3+Fe===3FeCl2 2FeCl3+Cu===2FeCl2+CuCl2(用于雕刻铜线路版)
2FeCl3+Zn===2FeCl2+ZnCl2 FeCl2+Mg===Fe+MgCl2
2FeCl3+H2S===2FeCl2+2HCl+S↓ 2FeCl3+2KI===2FeCl2+2KCl+I2
2,还原性:
2FeCl2+Cl2===2FeCl3 2Na2SO3+O2===2Na2SO4
3,与碱性物质的作用:
MgCl2+2NH3.H2O===Mg(OH)2↓+NH4Cl AlCl3+3NH3.H2O===Al(OH)3↓+3NH4Cl
FeCl3+3NH3.H2O===Fe(OH)3↓+3NH4Cl
4,与酸性物质的作用:
Na3PO4+HCl===Na2HPO4+NaCl Na2HPO4+HCl===NaH2PO4+NaCl
NaH2PO4+HCl===H3PO4+NaCl Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2↑ 3NaAlO2+AlCl3+6H2O===4Al(OH)3↓
3Na2CO3+2AlCl3+3H2O===2Al(OH)3↓+3CO2+6NaCl
5,不稳定性:
Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O NH4Cl===NH3↑+HCl↑
NH4HCO3===NH3↑+H2O+CO2↑ 2KNO3===2KNO2+O↑2
2Cu(NO3)3===2CuO+4NO2↑+O2↑ 2KMnO4===K2MnO4+MnO2+O2↑
2KClO3===2KCl+3O2↑ 2NaHCO3===Na2CO3+H2O+CO2↑
Ca(HCO3)2===CaCO3↓+H2O+CO2↑ CaCO3===CaO+CO2↑
MgCO3===MgO+CO2↑
1,氧化性:
(氧化性:HClO>HClO2>HClO3>HClO4,但浓,热的HClO4氧化性很强)
2H2SO4(浓)+C===CO2↑+2SO2↑+2H2O 2H2SO4(浓)+S===3SO2↑+2H2O
H2SO4+Fe(Al) 室温下钝化
6H2SO4(浓)+2Fe===Fe2(SO4)3+3SO2↑+6H2O 2H2SO4(浓)+Cu===CuSO4+SO2↑+2H2O
H2SO4(浓)+2HBr===SO2+Br2+2H2O H2SO4(浓)+2HI===SO2↑+I2+2H2O
H2SO4(稀)+Fe===FeSO4+H2↑ 2H2SO3+2H2S===3S↓+2H2O
4HNO3(浓)+C===CO2+4NO2↑+2H2O 6HNO3(浓)+S===H2SO4+6NO2↑+2H2O
5HNO3(浓)+P===H3PO4+5NO2↑+H2O 6HNO3+Fe===Fe(NO3)3+3NO2↑+3H2O
4HNO3+Fe===Fe(NO3)3+NO↑+2H2O
2,还原性:
H2SO3+X2+H2O===H2SO4+2HX (X表示Cl2,Br2,I2)
2H2SO3+O2===2H2SO4 5H2SO3+2KMnO4===2MnSO4+K2SO4+2H2SO4+3H2O
H2SO3+2FeCl3+H2O===H2SO4+2FeCl2+2HCl
3,酸性:
H2SO4(浓) +CaF2===CaSO4+2HF↑ H2SO4(浓)+NaCl===NaHSO4+HCl↑
H2SO4(浓) +2NaCl===Na2SO4+2HCl↑ H2SO4(浓)+NaNO3===NaHSO4+HNO3
3H2SO4(浓)+Ca3(PO4)2===3CaSO4+2H3PO4
2H2SO4(浓)+Ca3(PO4)2===2CaSO4+Ca(H2PO4)2
2HNO3+CaCO3===Ca(NO3)2+H2O+CO2↑
(用HNO3和浓H2SO4不能制备H2S,HI,HBr,(SO2)等还原性气体)
4H3PO4+Ca3(PO4)2===3Ca(H2PO4)2(重钙)
H3PO4(浓)+NaBr===NaH2PO4+HBr H3PO4(浓)+NaI===NaH2PO4+HI
4,不稳定性:
2HClO===2HCl+O2↑ 4HNO3===4NO2↑+O2↑+2H2O
H2SO3===H2O+SO2↑ H2CO3===H2O+CO2↑
H4SiO4===H2SiO3+H2O
1,还原性:
4HCl(浓)+MnO2===MnCl2+Cl2↑+2H2O 2H2O+2F2===4HF+O2
2H2S+3O2(足量)===2SO2+2H2O 4NH3+5O2===4NO+6H2O
2H2S+O2(少量)===2S↓+2H2O 2H2S+SO2===3S↓+2H2O
H2S+H2SO4(浓)===S↓+SO2↑+2H2O 3H2S+2HNO3(稀)===3S↓+2NO↑+4H2O
2,酸性:
4HF+SiO2===SiF4+2H2O(此反应广泛应用于测定矿样或钢样中SiO2的含量)
H2S+CuCl2===CuS↓+2HCl H2S+2AgNO3===Ag2S↓+2HNO3
3,碱性:
NH3+HCl===NH4Cl NH3+HNO3===NH4NO3
2NH3+H2SO4===(NH4)2SO4
NH3+NaCl+H2O+CO2===NaHCO3+NH4Cl(此反应用于工业制备小苏打,苏打)
4,不稳定性:
2H2O===2H2↑+O2↑ 2H2O2===2H2O+O2↑ H2S===H2↑+S↓
四,非金属氧化物
低价态的还原性:
2SO2+O2===2SO3
SO2+Cl2+2H2O===H2SO4+2HCl SO2+Br2+2H2O===H2SO4+2HBr
SO2+I2+2H2O===H2SO4+2HI 2NO+O2===2NO2
2CO+O2===2CO2 CO+CuO===Cu+CO2
3CO+Fe2O3===2Fe+3CO2 CO+H2O===CO2+H2
氧化性:
SO2+2H2S===3S↓+2H2O
NO2+2KI+H2O===NO+I2+2KOH(不能用淀粉KI溶液鉴别溴蒸气和NO2)
CO2+2Mg===2MgO+C (CO2不能用于扑灭由Mg,Ca,Ba,Na,K等燃烧的火灾)
SiO2+2H2===Si+2H2O SiO2+2Mg===2MgO+Si
3,与水的作用:
SO2+H2O===H2SO3 SO3+H2O===H2SO4
3NO2+H2O===2HNO3+NO N2O5+H2O===2HNO3
P2O5+H2O===2HPO3 CO2+H2O===H2CO3
P2O5+3H2O===2H3PO4(P2O5极易吸水,可作气体干燥剂P2O5+3H2SO4(浓)===2H3PO4+3SO3)
4,与碱性物质的作用:
SO2+Ca(OH)2===CaSO3↓+H2O(不能用澄清石灰水鉴别SO2和CO2.可用品红鉴别)
SO3+MgO===MgSO4 SO3+Ca(OH)2===CaSO4↓ +H2O
CO2+2NaOH(过量)===Na2CO3+H2O CO2(过量)+NaOH===NaHCO3
CO2+Ca(OH)2(过量)===CaCO3↓+H2O 2CO2(过量)+Ca(OH)2===Ca(HCO3)2
CO2+2NaAlO2+3H2O===2Al(OH)3↓+Na2CO3 CO2+C6H5ONa+H2O===C6H5OH↓+NaHCO3
SiO2+CaO===CaSiO3 SiO2+2NaOH===Na2SiO3+H2O(常温下强碱缓慢腐蚀玻璃)
SiO2+Na2CO3===Na2SiO3+CO2↑ SiO2+CaCO3===CaSiO3+CO2↑
五,金属氧化物
1,低价态的还原性:
6FeO+O2===2Fe3O4 FeO+4HNO3===Fe(NO3)3+NO2↑+2H2O
2,氧化性:
MgO,Al2O3几乎没有氧化性,很难被还原为Mg,Al.一般通过电解制Mg和Al.
Fe2O3+3H2===2Fe+3H2O (制还原铁粉) Fe3O4+4H2===3Fe+4H2O
3,与水的作用:
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2↑(此反应分两步:Na2O2+2H2O===2NaOH+H2O2 ;
2H2O2===2H2O+O2↑. H2O2的制备可利用类似的反应 )
MgO+H2O===Mg(OH)2 (缓慢反应)
4,与酸性物质的作用:
Na2O+SO3===Na2SO4 Na2O+CO2===Na2CO3
Na2O+2HCl===2NaCl+H2O 2Na2O2+2CO2===2Na2CO3+O2↑
MgO+SO3===MgSO4 MgO+H2SO4===MgSO4+H2O
(Al2O3是两性氧化物)
Al2O3+2NaOH===2NaAlO2+H2O Al2O3+3H2SO4===Al2(SO4)3+3H2O
FeO+2HCl===FeCl2+3H2O Fe2O3+6HCl===2FeCl3+3H2O
Fe3O4+8HCl===FeCl2+2FeCl3+4H2O
2Na+H2===2NaH 4Na+O2===2Na2O
2Na2O+O2===2Na2O2 2Na+O2===Na2O2
2Na+S===Na2S(爆炸) 2Na+2H2O===2NaOH+H2↑
4Na+TiCl4(熔融)===4NaCl+Ti Mg+Cl2===MgCl2
2Mg+O2===2MgO 2Mg+TiCl4(熔融)===Ti+2MgCl2
Mg+2H2O===Mg (OH)2+H2↑ Mg+H2SO4===MgSO4+H2↑
2Mg+CO2===2MgO+C 2Al+3Cl2===2AlCl3
4Al+3O2===2Al2O3(钝化) 4Al+3MnO2===2Al2O3+3Mn
2Al+Cr2O3===Al2O3+2Cr 2Al+3FeO===Al2O3+3Fe
2Al+Fe2O3===Al2O3+2Fe 2Al+3H2SO4===Al2(SO4)3+3H2↑
2Al+6HCl===2AlCl3+3H2↑ Al+4HNO3(稀)===Al(NO3)3+NO↑+2H2O
2Al+6H2SO4(浓)===Al2(SO4)3+3SO2↑+6H2O (Al,Fe在冷,浓的H2SO4,HNO3中钝化)
2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 2Fe+3Br2===2FeBr3
Fe+I2===FeI2 Fe+S===FeS
3Fe+4H2O(g)===Fe3O4+4H2 Fe+2HCl===FeCl2+H2↑
Fe+CuCl2===FeCl2+Cu Fe+SnCl4===FeCl2+SnCl2
(铁在酸性环境下,不能把四氯化锡完全还原为单质锡 Fe+SnCl2==FeCl2+Sn)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com