
题目列表(包括答案和解析)
17. 硝酸铅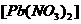 的稀溶液中滴入几滴稀Na2SO4,生成白色PbSO4沉淀,再滴入数滴饱和醋酸钠溶液,微热,并不断搅拌,沉淀慢慢溶解。以上发生的都是复分解反应,写出反应过程的离子方程式:___________。试推测第二步离子反应发生的原因是___________。
的稀溶液中滴入几滴稀Na2SO4,生成白色PbSO4沉淀,再滴入数滴饱和醋酸钠溶液,微热,并不断搅拌,沉淀慢慢溶解。以上发生的都是复分解反应,写出反应过程的离子方程式:___________。试推测第二步离子反应发生的原因是___________。
16. 某河道两旁有甲、乙两厂,它们排放的工业废水中共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是________。
乙厂的废水中含有另外三种离子。如果加一定量________(选填:“活性炭”、“硫酸亚铁”、“铁粉”),可以回收其中的金属_____(填写元素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的___________(填写离子符号)转化为沉淀,经过滤后的废水主要含___________,可用来浇灌农田。
15. 在世纪交替之时,某国炼金废水泄入尼罗河,导致大量鱼类等水生生物死亡,沿河居民长期停止使用此水源,酿成世界污染事件。炼金废水中含有络离子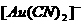 ,其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强。回答下列问题:
,其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强。回答下列问题:
(1)剧毒物HCN的结构式为_________,其水溶液酸性很弱,可知NaCN溶液pH_____7(填“>”,“=”,“<”)。
(2)与弱电解质碳酸的电离方程式相似,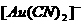 也存在着两步电离,其一级电离方程式为_________________。
也存在着两步电离,其一级电离方程式为_________________。
(3)处理这种废水时是在碱性条件下NaClO将CN-氧化为CO32-和N2,其离子方程式为___________________。在酸性条件下,ClO-也能氧化CN-,但实际处理废水时却不在酸性条件下进行的主要原因是_________________。
14. 已知:2Fe2++Br2=2Fe3++2Br-,2I-+2Fe3+=2Fe2++I2
试回答下列问题:
(1)试比较Fe2+、I-、Br-的还原性强弱。
(2)少量Cl2通入FeBr2溶液中,写出反应的离子方程式。
(3)过量Cl2通入FeBr2溶液中,写出反应的离子方程式。
13. 在含有Na+、Mg2+、HCO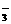 、SO
、SO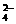 的稀溶液中,它们的物质的量之比为2:1:2:1。
的稀溶液中,它们的物质的量之比为2:1:2:1。
(1)向该溶液中滴加酚酞试液数滴,溶液呈淡粉红色,有关反应的离子方程式为_____。
(2)充分加热(1)步所得的溶液,加热的过程中观察到的现象有___________;完全反应后,溶液呈_________色,有关反应的离子方程式为_______________。
12. NaBH4是一种强还原剂。
(1)NaBH4极易溶于水,并与水剧烈反应放出H2,反应后硼以BO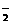 形式存在。写出反应的离子方程式:__________。实验表明,溶液酸性越强,生成H2的速度越快,其原因是_________________。
形式存在。写出反应的离子方程式:__________。实验表明,溶液酸性越强,生成H2的速度越快,其原因是_________________。
(2)在碱性条件下,NaBH4往往不是与水反应,而是与许多金属离子发生反应,硼仍以BO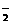 形式存在,例如冶金工业中,用NaBH4可使Au3+的废液中的Au3+还原。其离子方程式是___________。
形式存在,例如冶金工业中,用NaBH4可使Au3+的废液中的Au3+还原。其离子方程式是___________。
(3)在60年代,德国拜尔药厂用下面的反应把NaBH4的生产发展成工业规模。
Na2B4O7+Na+H2+SiO2--NaBH4+Na2SiO3
试配平这个方程式_____________ 。
11.(1)向NaHSO4溶液中,逐滴加入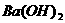 溶液至中性,写出发生反应的离子方程式:________。
溶液至中性,写出发生反应的离子方程式:________。
在以上中性溶液中继续滴加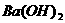 溶液,写出此步反应的离子方程式:______。
溶液,写出此步反应的离子方程式:______。
(2)向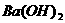 溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,写出反应的离子方程式:_________________。
溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,写出反应的离子方程式:_________________。
在以上溶液中,继续加NaHSO4溶液,写出此步反应的离子方程式:___________。
(3)向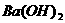 溶液中,逐滴加入明矾溶液至溶液中Ba2+恰好完全沉淀,其反应的离子方程式是:________。
溶液中,逐滴加入明矾溶液至溶液中Ba2+恰好完全沉淀,其反应的离子方程式是:________。
在上述溶液中,继续滴加明矾溶液,写出此步反应的离子方程式:_______。
10. 在c(HCO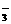 )=0.1 mol·L-1的溶液中,可以大量共存的离子组是( )
)=0.1 mol·L-1的溶液中,可以大量共存的离子组是( )
A.
Al3+、NO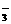 、NH
、NH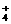 、Cl- B. Na+、SO
、Cl- B. Na+、SO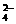 、K+、CH3COO-
、K+、CH3COO-
C. H+、Ba2+、Cl-、NO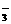 D.
Na+、CO
D.
Na+、CO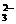 、K+、OH-
、K+、OH-
9. 下列各组离子能大量共存于同一溶液中,且加入过量NaOH溶液或少量稀硫酸时,都能产生白色沉淀的是( )
A.
Ba2+、Mg2+、NO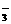 、CO
、CO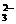 B.
Na+、Al3+、Cl-、AlO
B.
Na+、Al3+、Cl-、AlO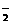
C. K+、Ba2+、Cl-、HCO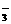 D.
NH
D.
NH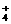 、Ba2+、Fe3+、Cl-
、Ba2+、Fe3+、Cl-
8. 下列各组离子的无色溶液可能跟镁粉反应,又能大量共存的是( )
A. K+、Cl-、SO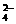 、NH
、NH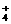 B.
Ca2+、Cl-、MnO
B.
Ca2+、Cl-、MnO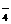 、Na+
、Na+
C.
AlO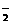 、Na+、Al3+、I- D. H+、Cl-、Ba2+、NO
、Na+、Al3+、I- D. H+、Cl-、Ba2+、NO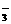
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com