
题目列表(包括答案和解析)
12.下列物质中的一氯代烷有三种的是
A.正己烷 B.2-甲基戊烷
C.2,2-二甲基丁烷 D.2,3-二甲基丁烷
11.下列各组数据中前者比后者大的是
A.pH=10的K2CO3溶液和pH=10的KOH溶液中由水电离出的OH-离子浓度
B.0.1mol·L-1的CH3COOH溶液与1.0mol·L-1的CH3COOH溶液中c(H+)
C.Na2CO3溶液的HCO3-和OH-的数目
D.纯水在20℃和100℃时的pH
10.现将V1 L pH=10的NaOH溶液和V2 L pH=5的H2SO4溶液混合,得(V1+V2)L pH=8的溶液,那么V1∶V2为:
A.1∶9 B.2∶11 C.1∶4 D.11∶2
9.曾在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过H2O。以下叙述正确的是
A.铝热剂就是单指Fe2O3粉和铝粉的混合物
B.检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品--粉碎--加水溶解--过滤--向滤液中滴加KSCN溶液
C.分别还原amol Fe2O3所需H2、Al、CO物质的量之比为3∶2∶3
D.明矾属硫酸盐,是纯净物
8.下列离子方程式正确的是
A.氢碘酸和硝酸银溶液的反应:HI+Ag+=AgI↓+H+
B.氨气通入氢氟酸溶液中:NH3+H+=NH4+
C.向碳酸氢镁溶液中加入过量烧碱:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O
D.向NaAlO2溶液中通入少量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
7.反应4NH3(g)+5O2(g)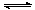 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或产物的生成速率)可表示为
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或产物的生成速率)可表示为
A.v(NH3)=0.010 mol·L-1·s-1 B.v(O2)=0.0010 mol·L-1·s-1
C.v(NO)=0.0010 mol·L-1·s-1 D.v(H2O)=0.045 mol·L-1·s-1
6.在含0.01mol的明矾[KAl(SO4)2·12H2O]的溶液中逐滴加入含有0.02mol的Ba(OH)2溶液,下列判断正确的是
A、先出现沉淀,后来全部溶解
B、最终得到的沉淀只有硫酸钡
C、当Al3+、SO42-全部沉淀时,得到的沉淀质量最大
D、当SO42-完全沉淀时,得到的沉淀物质的量最大
5.某无色溶液pH=1,投入铝片有氢气放出,则溶液中下列各组离子能大量共存的是
A.NH4+、Al3+、SO42-、Br- B.K+、Na+、Cl-、NO3-
C.Mg2+、Na+、OH-、Cl- D.K+、NH4+、SO42-、HCO3-
4.在一定条件下,可逆反应X(g)+2Y(g)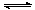 2Z(g)达到平衡时,测得Y的转化率为20%,X的转化率为50%,则反应开始时,充入容器中X和Y物质的量之比为
2Z(g)达到平衡时,测得Y的转化率为20%,X的转化率为50%,则反应开始时,充入容器中X和Y物质的量之比为
A.1∶5 B.1∶4 C.1∶3 D.1∶2
3.铜制品上的铝质铆钉,在潮湿空气中易腐蚀的原因可描述为
A.形成原电池时,铝作负极
B.形成原电池时,铜作负极
C.形成原电池时,电流是由铝经导线流向铜
D.铝铆钉发生了化学腐蚀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com