
题目列表(包括答案和解析)
2.R表示某元素,且知下面的反应中各元素的化合价不变,RxOy+3H2SO4====R2(SO4)3+3H2O,则x、y的数值为x=_________,y=_________。
思路解析:根据质量守恒定律知,反应前后原子个数相等。?x=2,y=3。?
答案:2 3
1.在化学反应A+2B====C+2D中,m克A物质与n克B物质刚好完反应生成e克C物质,则同时生成D物质的克数是 ( )
A.m+ -e
B.m+2n-e
-e
B.m+2n-e
C.m+n-2e D.m+n-e
思路解析:根据质量守恒定律:D的生成物质量=m+n-e。
答案:D
3.化学方程式 2H2O+O2 2H2O中等号表示( )
2H2O中等号表示( )
A.水由氢气和氧气组成
B.参加反应的氢、氧分子数之和等于生成的水的分子数
C.参加反应的氢气、氧气质量之和等于生成的水的质量
D.参加反应的氢质量等于水中氢气的质量
思路解析:该方程式中等号表示参加反应方程式两边的物质的质量相等。
答案:C
快乐时光
迎新
新学期开始,我们高年级学生去车站迎接新同学。我见一小女生站在一个大箱子旁不知所措,便主动上前帮她提箱子。不料箱子重逾千斤,我又不好意思放下箱子,只好勉力支撑。才走了几步,那女生便对我说:“背不动就滚吧。”我一听此言,登时怒从心头起,放下箱子,怒视着她。那女生愣了几秒钟,才满脸通红地指着箱子的底部对我说:“我指的是轮子。”
30分钟训练 (巩固类训练,可用于课后)
2.下列化学方程式中,完全正确的是( )
A.P+O2 P2O5
B.C+2O
P2O5
B.C+2O CO2
CO2
C.Mg2+O2 2MgO
D.3Fe+2O2
2MgO
D.3Fe+2O2 Fe3O4
Fe3O4
思路解析:A没有配平;B中应该写成氧分子而不是氧原子;C中镁的化学计量数应该写在镁的元素符号前而不能写在右下角,表示意义不对;D符合化学方程式的书写规则。
答案:D
1.配平下列反应的化学方程式:
(1)NH3+ Cl2--N2+HCl
(2)C2H2+ O2 --CO2+ H2O
(3)Fe2O3+ CO --Fe +CO2
思路解析:根据化学方程式配平的步骤,结合质量守恒定律,可以得到答案。
答案:(1)2NH3+3Cl2====N2+6HCl
(2)2C2H2+ 5O2 4CO2+
2H2O
4CO2+
2H2O
(3)Fe2O3+3CO 2Fe +3CO2
2Fe +3CO2
2.质量守恒定律说明化学反应前后各物质的质量总和相等,这是因为在一切化学反应里,反应前后____________没有改变,____________也没有增减。书写和配平化学方程式的基础是根据质量守恒定律。
思路解析:质量守恒定律是化学反应方程式配平的基础,反应前后参加反应的各物质的原子总数没有改变,总质量也没有改变。
答案:参加反应的物质的原子总数物质的总质量
10分钟训练 (强化类训练,可用于课中)
1.化学方程式C+O2====CO2表示:①____________;②____________;③____________。
思路解析:本题考查化学方程式的意义。
答案:①碳与氧气在点燃的条件下生成二氧化碳②一个碳原子与一个氧气分子生成一个二氧化碳分子③每12份质量的碳与每32份质量的氧气完全反应,生成44份质量的二氧化碳。
11.根据质量守恒定律,6 g镁和8 g氧气充分反应,可生成14 g氧化镁。这种说法正确吗?为什么?如不正确,请加以改正。
解答:在化学反应中,各反应物之间是按照一定的质量比相互作用的。因此,质量守恒定律中“参加化学反应的各物质的质量总和”就不是任意比例的反应物的质量的简单加和,而应是按一定的质量比进行反应的各反应物的质量总和。所以本题简单地用:6 g+ 8 g=14 g的计算方法就得出生成物氧化镁的质量,是错误的。
可以用以下方法求出氧化镁的质量:
解:2Mg+O2 2MgO
2MgO
2×2432
68
由于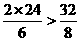 ,所以氧气过量。
,所以氧气过量。
设6 g镁能与氧气反应的质量为x。
2Mg+O2 2MgO
2MgO
48 32
6 g x
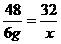 ,x=4 g
,x=4 g
生成氧化镁的质量:6 g + 4 g=10 g。
所以上述说法可以这样改正:
根据质量守恒定律,6 g镁和4 g氧气恰好完全反应后,可以生成10 g氧化镁。
10.用100克KClO3和MnO2的混合物制取氧气,反应前测得MnO2占混合物总质量的25%,反应一段时间后,又测得MnO2占30%。求:此时分解的KClO3的质量是多少?制得的氧气的质量是多少?
思路解析:反应前:
MnO2的质量为:100克×25%=25克
KClO3的质量为:100克-25克=75克
反应后:
混合物的质量为:25克÷30%=83.3克
生成氧气的质量为:100克-83.3克=16.7克
设已分解的KClO3的质量为x。
2KClO3 2KCl+3O2↑
2KCl+3O2↑
245 96
x 16.7克

x=42.6克
答案:分解的KClO3的质量为42.6克,制得氧气16.7克。
9.一定质量的镁和碳酸镁混合物,经高温煅烧,直到质量不再变化为止。发现反应前后总质量不变,求原混合物中镁粉的质量分数。
思路解析:这里包括两个反应:
2Mg+O2 2MgO
2MgO
MgCO3 MgO+CO2↑
MgO+CO2↑
对于镁粉来说,生成物质量增加了,增加部分是反应氧气的质量。对于碳酸镁来说,生成物质量减少了,减少部分是CO2的质量,且增加量等于减少量,这样不难计算。同学们不妨动手试试。
答案:44%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com