
题目列表(包括答案和解析)
4、为揭示原子光谱是线状光谱这一事实,玻尔提出了核外电子的分层排布理论,下列说法中,不符合这一理论的是( )
A、电子绕核运动具有特定的半径和能量
B、电子在特定半径的轨道上运动时不辐射能量
C、电子跃迁时,会吸收或放出特定的能量
D、提示了氢原子光谱存在多条谱线
3、使用微波炉加热,具有使受热物质均匀、表里一致、速度快、热效率高等优点。其工作原理是通电炉内的微波场以几亿的高频改变外电场的方向,水分子因而能迅速摆动,产生热效应,这是因为( )
A、水分子具有极性共价键 B、水分子中有共电子对
C、水由氢、氧两种元素组成 D、水分子是极性分子
2、氢原子的电子云图中小黑点表示的意义是( )
A、1个小黑点表示一个电子
B、小黑点的多少表示电子个数的多少
C、表示电子运动的轨迹
D、表示电子在核外空间出现机会的多少
1、关于原子结构模型的演变过程,正确的是( )
A、汤姆逊原子模型→道尔顿原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型
B、汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型→道尔顿原子模型
C、道尔顿原子模型→卢瑟福原子模型→汤姆逊原子模型→玻尔原子模型→量子力学模型
D、道尔顿原子模型→汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型
《化学与生活》选做题为第30-33题,标记“★”:
★30、(8分)下表是某食品包装袋上的说明
|
品 名 |
浓缩菠萝汁 |
|
配 料 |
水.浓缩菠萝汁.蔗糖.柠檬酸.黄原胶.甜蜜素.维生素C,菠萝香精.柠檬黄.日落黄.山梨酸钾等 |
|
果汁含量 |
≥80% |
|
生产日期 |
标于包装袋封口上 |
从表中的配料中分别选出一种物质填在相应的横线上。
其中属于着色剂的有 ,属于调味剂的有 ,
属于防腐剂的有 ,属于营养强化剂的有 。
★31、(4分)维生素C(C6H8O6)主要存在于 和 中,它能促进人体生长发育,增强人体对疾病的抵抗力。
★32、(2分)青霉素是一种重要的抗生素,由于可能会出现过敏反应,为患者的生命安全,使用前必须进行 。
★33、(6分)某药品标签上贴有OTC,它表示 ,若是R标记则表示 ,平时我们到药店能买到的药如阿司匹林属于 。
《有机化学基础》选做题为第30-31题,标记“◆”:
◆30、(12分)已知下列数据:
|
物质 |
熔点(℃) |
沸点(℃) |
密度 |
|
乙 醇 |
-117.0 |
78.0 |
0.79 |
|
乙 酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
|
浓硫酸(98%) |
-- |
338.0 |
1.84 |
学生在实验室制取乙酸乙酯的主要步骤如下:
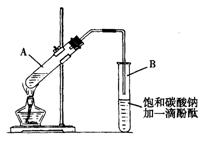 ①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;②按下图连接好装置(气密性良好),用小火均匀地加热装有混合溶液的大试管5-10 min;③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层;④分离出乙酸乙酯层、洗涤、干燥。
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;②按下图连接好装置(气密性良好),用小火均匀地加热装有混合溶液的大试管5-10 min;③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层;④分离出乙酸乙酯层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为: ;
写出制取乙酸乙酯的化学方程式:
;
(2)上述实验中饱和碳酸钠溶液的作用是(填字母): ;
A.中和乙酸和乙醇. B.中和乙酸并吸收部分乙醇.
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出.
D.加速酯的生成,提高其产率.
(3)步骤②中需要小火均匀加热操作,其主要理由是:
;
分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,可通过洗涤除去(填名称) 。
◆ 31、(8分)取3.40ɡ只含羟基、不含其他官能团的液态饱和多元醇,置于5.00L的氧气中,经点燃,醇完全燃烧。反应后气体体积减少0.560L,将气体经CaO吸收,体积又减少2.8L(所有体积均在标况下测定)。 则:3.4ɡ醇中C、H、O的物质的量分别为:
C____; H______; O_______;该醇中C、H、O的原子个数之比为___________。
(请写出计算过程,无过程不得分)
江阴市青阳中学2006-2007学年度第一学期期末考试模拟试题
29、(8分)常温下,A是双原子分子气态单质,其密度为3.17g/L(标准标况下),B、C、D都是含A元素的化合物,转化关系如下图所示:
 (1)分别写出A、B、C、D的化学式:
(1)分别写出A、B、C、D的化学式:
A B
C D
(2) 试写出有关化学方程式:
A→B
D→A 。
28、(6分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为:
;
(2)漂白粉的有效成分是(填化学式) ;
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 ;
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) 。
27、(10分)(1)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):___________________________________________。
②容量瓶:________________________________________________________。
(2)何除去下列物质中的杂质(括号内为杂质),请在横线上填入适当的试剂或方法:
①NaCl溶液(Na2CO3)
②NaOH溶液(Na2CO3)
③Na2CO3固体(NaHCO3)
④CO2气体(HCl)
(3)下列有关化学实验操作中“先”与“后”的说法正确的是 (填字母代号)。
A.用排水法收集气体后,先撤酒精灯,后移出导管
B.给试管加热时,先均匀加热,后局部加热
C.碱液沾在皮肤上,先用稀醋酸溶液中和,后用水洗
D.点燃可燃性气体(如H2、CO等)时,都要先检验气体纯度,后点燃
26、(6分)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③水银 ④蔗糖 ⑤冰醋酸(固态醋酸晶体)⑥KNO3溶液 填空回答(填序号):
(1)以上物质能导电的是 ;
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是 。
18、配制100mL、1.0mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是
A.容量瓶使用前经蒸馏水清洗后没有干燥
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.俯视确定凹液面与刻度线相切
D.用敞口容器称量NaOH且时间过长
《化学与生活》选做题为第19-25题,标记“★”:
★19、“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制的易拉罐、铜导线等可以归为一类加以回收,它们属于
A.氧化物 B.盐 C.金属或合金 D.碱
★20、绿色化学实验是在绿色化学的思想指导下,对常规实验进行改革而形成的实验的新方法。它能极大地减少或消除实验中的“三废”、污染和浪费等。下列符合绿色化学实验的操作是
A.将一氧化碳还原氧化铜的尾气直接排入空气中 B.将锌和稀硫酸反应后的废液直接倒入下水道中 C.将跟氧气反应后剩余的硫磺放在空气里燃烧完
D.将氯酸钾和二氧化锰共热残余物回收分离
★21、生活中处处有化学。请根据你所学过的化学知识,判断下列说法中错误的是
A.医疗上常用体积分数为75%的酒精作消毒剂
B.为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒
C.在家里可用食盐来腌制食品,延长保鲜时间
D.使用液化石油气做燃料可以杜绝厨房污染
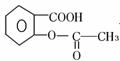 ★22、阿司匹林是一种常用的解热镇痛药,其结构如右图,推断正确的是
★22、阿司匹林是一种常用的解热镇痛药,其结构如右图,推断正确的是
A.可以与碱发生反应 B.属于氨基酸
C.该物质易溶于水 D.可以发生化合反应
★23、下列药物类型中由于过度使用导致人类面临无药可用的危机的是
A.中成药 B.抗生素 C.抗酸药 D.解热镇痛药
★24、1997年,第一只“克隆羊”在英国诞生,“克隆羊”的关键技术之一是找到一些特殊的酶,它们能激活普通体细胞,使之像生殖细胞一样发育成个体。下列有关酶的叙述错误的是
A.酶是具有催化功能的蛋白质
B.酶的催化作用具有选择性和专一性
C.酶通常在强酸或强碱的条件下发挥作用
D.高温或紫外线的照射会降低酶的活性
★25、现有三种常见治疗胃病药品的标签:

① ② ③
药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是
A.③>②>① B.①>②>③
C.②>③>① D.①=②=③
《有机化学基础》选做题为第19-25题,标记“◆”:
◆19、下列说法正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.糖类、油脂、蛋白质都是由C、H、O三种元素组成的
C.糖类、油脂、蛋白质都是高分子化合物
D.油脂有油和脂肪之分,但都属于酯
◆20、下列有关乙酸的性质的叙述错误的是
A.有强烈刺激性气味的无色液体
B.乙酸的沸点比乙醇高
C.乙酸的酸性比碳酸强,它能与碳酸盐反应
D.在酯化反应时,乙酸分子羟基中的氢原子跟醇分子中的羟基结合成水
◆21、一种气态烷烃和一种气态烯烃的混合物9 g,其密度是相同条件下氢气密度的11.25倍,当混合气体通过足量溴水时,溴水增重4.2 g,则这两种气态烃是
A.甲烷和乙烯 B.乙烷和乙烯 C.甲烷和丙烯 D.甲烷和丁烯
◆22、苯的结构式可用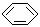 来表示,下列关于苯的叙述中正确的是
来表示,下列关于苯的叙述中正确的是
A.苯主要是以石油为原料而获得的一种重要化工原料
B.苯中含有碳碳双键,所以苯属于烯烃
C.苯分子中6个碳碳化学键完全相同
D.苯可以与溴水、高锰酸钾溶液反应而使它们褪色
◆23、已知二氯苯的同分异构体有三种,从而可以推知四氯苯的同分异构体数目是
A.1 B.2 C.3 D.4
◆24、标准状况下,0.56 L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28g(假设C2H4完全被吸收),则乙烯占混合气体体积的
A.20% B.40% C.60% D80%
◆25、一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2、H2O的总质量为27.6 g,若其中水的质量为10.8g则CO的质量为
A、1.4g B、2.2g C、4.4g D 、2.2 g到4.4克之间
第Ⅱ卷(非选择题 共50分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com