
题目列表(包括答案和解析)
2.C 分析:阳极:Ag+ + e- === Ag
1mol 1mol 108g
1.D 分析:物质的选取一要考虑能否和Cl2反应,二要考虑其本身或反应产物对人的健康的影响
25.(7分)两根镍棒分别与电源正负极相连,并都插入NiSO4溶液中。若电流强度为I,通电时间为ts,结果阳极失重mg。已知每个电子的电量为1.6×10-19C,则可推知阿伏加德罗常数为多少?
第4单元测试答案
24.(12分)(1)当电源通过2L6%的KOH溶液(ρ==1.05g/mL)时,溶液的浓度改变了2%,此时阳极析出的物质是什么?质量为多少克?
(2)若电解后溶液不小心混入KCl杂质,为了除去杂质又进行电解,当有5.6L(标态)Cl2析出,可认为电解作用是完全的,求最后所得溶液中KOH的质量分数为多少?
23.(8分)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量的问题。解决方法之一是把这些陶土和水一起搅拌,使微粒直径在10-9m-10-7m之间,然后插入两根电极,接通直流电源,这时阳极聚集________,阴极聚集_______,理由是_______________________________________________________________________。
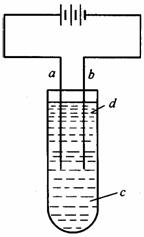
22.(14分)由于Fe(OH)2极易被氧化,所以实验很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。应用如图所示电解实验可制得白色纯净的Fe(OH)2沉淀。两电极的材料分别为石墨和铁。
(1)a电极材料应为________,电极反应式为_________________________。
(2)电解液c可以是(填编号)__________________。
A.纯水 B.NaCl溶液
C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为_________________,在加入苯之前对c应做何简单处理?_____________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施是(填编号)_________
A.改用稀硫酸作电解液 B.适当增大电源的电压
C.适当减小两电极间距离 D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为
____________________________________________。
21.(9分)图中每一方框中的字母代表一种反应物或生成物:
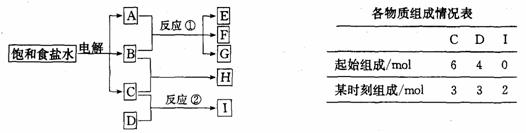
 物质A跟B反应生成E、F和G,物质C跟D反应生成I,某温度下该反应起始和某时刻的反应混合物组成如上表,请填写下列空白:
物质A跟B反应生成E、F和G,物质C跟D反应生成I,某温度下该反应起始和某时刻的反应混合物组成如上表,请填写下列空白:
(1)物质H的分子式是_________________
(2)反应①的化学方程式是_____________________________________________。
(3)反应②的化学方程式(须注明反应条件)是________________________________。
20.将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比是 ( )
A.1:2:3 13.3:2:1 C.6:3:1 D.6:3:2
第四单元 电解原理及其应用
单元测试
____班学生_________得分 _________
一题答题表
19.下列过程①电离②电解③电镀④电泳⑤电化腐蚀,需通电后才可进行的是 ( )
A.①②③ B.②③④ C.③④⑤ D.①②③④⑤
18.下列关于电解精炼铜的叙述中不正确的是 ( )
A.粗铜板体:阳极
B.电解时,阳极发生氧化反应,而阴极发生的反应为Cu2++2e-=Cu
C.粗铜中所含Na、Fe、Zn等杂质,电解后以单质形式沉积槽底,形成阳极泥
D.电解铜的纯度可达99.95%-99.98%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com