
题目列表(包括答案和解析)
2.向纯水中加入少量NaHSO4晶体,若温度不变,则溶液中
A. 水电离出的H+大于水电离出的OH-浓度
B. c(H+).c(OH-)乘积增大
C. 酸性增强
D. OH-浓度减小
1.下列各种离子,不能破坏水的电离平衡的是( )
A. 所有离子中半径最小的离子
B. 最外层电子排布和氖原子相同的+1阳离子
C. NaOH溶于水电离出的离子
D. NaHSO4溶于水电离出的离子
9.O.55 mol·L-1·s-1 5 mol·L-1
8.O.1 mol·L-1·min O.05 mol·L-1·min-1
7.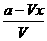 mol.L-1.min-1
mol.L-1.min-1
1.B 2.A 3.C 4.CD 5.D 6.A
2.1化学反应速率第一课时
9.对于反应:4FeS2+llO2====2Fe2O3+8S02,当生成S02的速率为O.4 mol.L-1·s-1,则O2的减少速率为_________,测得4 s后,O2的浓度为2.8 mol.L-1,则O2的起始浓度为_____________.
8.可逆反应2SO2(g)+02(g)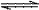 2SO3(g)如果S02的起始浓度为2 mol·L-1,2 min后,S02的浓度为1.8 mol·L-1,则用S02的浓度变化表示的反应速率为__________,用O2的浓度变化表示的反应速率为__________。
2SO3(g)如果S02的起始浓度为2 mol·L-1,2 min后,S02的浓度为1.8 mol·L-1,则用S02的浓度变化表示的反应速率为__________,用O2的浓度变化表示的反应速率为__________。
7.取a mol A和b mol B置于V L容器内,发生可逆反应:aA(g)+bB(g)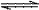 cC(g)+dD(g)1
min后,测得A的浓度为x mol.L-1,这段时间内反应的平均速率若以物质A的浓度变化来表示,应为___________。
cC(g)+dD(g)1
min后,测得A的浓度为x mol.L-1,这段时间内反应的平均速率若以物质A的浓度变化来表示,应为___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com