
题目列表(包括答案和解析)
13. 对于可逆反应x+y
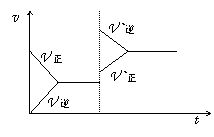
对于可逆反应x+y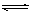 z+w达平衡后,在其他条件不变的情况下,增大压强,反应速率变化如右图。
z+w达平衡后,在其他条件不变的情况下,增大压强,反应速率变化如右图。
判断四种物质的状态正确的是
A.四种物质均为气体
B.x、y均为气体,z、w中有一种为气体
C.z、w中有一种为气体,x、y皆非气体
D.z、w均为气体,x、y中有一种为气体
12.在密闭容器中发生下列反应:aX(g)+bY(g) 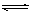 cZ(g)+dW(g) 反应达平衡后将气体体积缩小为原体积的1/2,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列说法正确的是
cZ(g)+dW(g) 反应达平衡后将气体体积缩小为原体积的1/2,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列说法正确的是
A.平衡向逆反应方向移动 B. a+b>c+d
C.Z的体积分数增大 D.X的转化率减小
11.反应NH4HS(s) 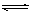 NH3(g)+H2S(g)在某一温度下达到平衡时,下列各种情况中,不能使平衡发生移动的是
NH3(g)+H2S(g)在某一温度下达到平衡时,下列各种情况中,不能使平衡发生移动的是
A.其他条件不变,通入SO2气体 B.加入一部分NH4HS固体
C.保持容器体积不变,充入氮气 D.保持容器体积不变,通入氯气
10.下列离子方程式中正确的是
A.氢氧化钡溶液和过量的硫酸氢钠溶液反应
Ba2++OH-+H++SO42-==BaSO4↓+H2O
B.将过量二氧化硫通入氢氧化钠溶液
SO2+2OH- ==SO32-+H2O
C.将氯气通入氯化亚铁溶液中
2Fe2++Cl2==2Fe3++2Cl-
D.三氯化铁在溶液中发生水解反应
Fe3++3H2O==Fe(OH)3↓+3H+
9.用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减少的是
A. B.
B.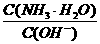
C. C(H+)和C(OH-)的乘积 D.
8.已知溶液中水电离出来的氢离子浓度为10-13mol/L,在此溶液中肯定能大量共存的离子组是
A. Na+、Ba2+、Cl-、NO3- B.SO32-、Cl-、Na+、SO42-
C.NH4+、K+、NO3-、SO42- D.Al3+、Cl-、Na+、AlO2-
7.下列有关叙述不正确的是
A.纯净的强电解质在液态时有的导电,有的不导电
B.同温度、同浓度时,弱电解质的导电能力一定比强电解质的导电能力弱
C.电解质溶液导电能力的强弱,取决于溶液中电解质的物质的量浓度
D.已达到电离平衡的溶液,当温度升高时电离平衡会发生移动
6.用0.1mol/L的盐酸跟0.06mol/L氢氧化钡溶液等体积混合,则混合溶液的pH为
A. 2 B. 1.7 C. 12 D. 12.3
5.在含有酚酞的0.1mol/L氨水中加入少量的NH4Cl晶体,则溶液颜色
A.变蓝色 B.变深 C.变浅 D.不变
3.可充分说明可逆反应:P(g)+Q(g)  R(g)+S(g),在恒温下达到平衡状态的标志是
R(g)+S(g),在恒温下达到平衡状态的标志是
A.反应器内压强不随时间变化而变化
B.反应器内P、Q、R、S四种气体共存
C.生成P的速率与生成S的速率相等
D.生成1molP同时必有1molQ生成
 4.反应2X(g)+Y(g)
4.反应2X(g)+Y(g) 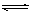 2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如右图。下列判断正确的是
2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如右图。下列判断正确的是
A. T1<T2 , 正反应为放热反应
B. T1>T2 ,正反应为吸热反应
C. T1>T2 ,逆反应为吸热反应
D. T1<T2 ,逆反应为放热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com