
题目列表(包括答案和解析)
17、(1)C→A→B→D→E;
(2)眼睛平视液面最低点;(3)便于观察溶液颜色变化;(4)零刻度稍靠下的某一确定刻度;充满溶液;(5)偏高;碱的物质的量浓度大于确定体积所给定的值,导致多消耗标准酸溶液;(6)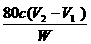 %。
%。
16、900,1000,100
15、3<pH<5
14、小于;温度升高水的电离度增大,而pH减小。
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
BD |
BC |
A |
D |
C |
D |
C |
C |
C |
D |
D |
CD |
D |
18.250 mL pH=12的某一元强碱(MOH)溶液与250 mL 0.025 mol·L-1 的硫酸溶液相混合, 假设混合后液体体积为500 mL。试求:
(1)混合液的pH;
(2)若原250 mL一元强碱中含溶质0.1 g, 则M的相对原子质量为多少?
(3)若给混合液中分别滴入几滴甲基橙、无色酚酞、紫色石蕊试液,则溶液的颜色分别是什么?
《电离平衡》复习练习二 答案
17.某烧碱样品中含有少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作:
(A)在250mL的容量瓶中定容配制250mL烧碱溶液;
(B)用移液管移取25mL烧碱溶液于锥形瓶中,并滴入几滴甲基橙作指示剂;
(C)在托盘天平上准确称取烧碱样品Wg ,在烧杯中用蒸馏水溶解;
(D)将物质的量浓度为cmol·L-1的标准硫酸溶液装入已润洗过的酸式滴定管中,调整液面并记下起始读数为V1mL;
(E)在锥形瓶下垫一张白纸,滴定至橙色为止,记下读数为V2mL。
就此完成下列问题:
(1)正确操作步骤是(用编号字母填空)___→____→____→D→____;
(2)观察滴定管里液面的高度时应注意:____________________。
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用是____________________。
(4)D步骤的操作中液面应调整到___________________________________,尖嘴部分应该________________________。
(5)某学生实验时把锥形瓶用待测烧碱溶液润洗,则测定的烧碱溶液的浓度偏高还是偏低________;其原因是_______________________________________________。
(6)该烧碱样品纯度的计算公式是________________________。
16.有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。
(1)如果加入蒸馏水,就加入________ mL
(2)如果加入pH = 10的NaOH溶液,应加入_________ mL
(3)如果加入0.008 mol/L HCl溶液,应加入__________ mL
15.将pH=3的弱酸溶液稀释100倍,该溶液的pH范围为:__________________。
14.在95℃时,纯水的pH (填“大于”“小于”“等于”)7,所选择的理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com