
题目列表(包括答案和解析)
12.下列变化规律与共价键键能大小有关的是:
A、F2、Cl2、Br2、I2的熔沸点逐渐升高
B、HF、HCl、HBr、HI的稳定性逐渐减弱
C、金刚石的硬度、熔点、沸点都高于晶体硅
D、NaF、NaCl、NaBr、NaI熔点依次降低
11.一定能在下列溶液中大量共存的离子组是
A、pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl-
B、能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32-
C、含有大量Fe3+的溶液:SCN-、I-、K+、Br-
D、澄清透明的无色溶液中:ClO-、MnO4-、Al3+、SO42-
10. 关于如图所示装置的叙述,正确的是
关于如图所示装置的叙述,正确的是
A、铜是阳极,铜片上有气泡产生
B、锌片质量逐渐减少
C、电流从锌片经导线流向铜片
D、氢离子在铜片表面被还原
9.配合物的空间构型和配位数之间有着密切的关系,配位数为4的配合物空间立体构型是
A、四面体 B、正八面体 C、平面四边形 D、三角形
8.下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)===CO2(g);△H1 C(s)+O2(g)===CO(g);△H2
②S(s)+O2(g)===SO2(g);△H3 S(g)+O2(g)===SO2(g);△H4
③H2(g)+O2(g)===H2O(l);△H5 2H2(g)+O2(g)===2H2O(l);△H6
④CaCO3(s)===CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)===Ca(OH)2(s);△H8
A、① B、④ C、②③④ D、①②③
7.有组成是CrCl3·6H2O的配合物,中心原子Cr3+的配位数为6,Cl-、H2O均可作配体,向含有0.1mol该配合物的溶液中,加入足量硝酸银溶液,共得到14.35g沉淀,则该配合物的化学式是
A、[Cr(H2O)6]Cl3 B、[Cr(H2O)4Cl2]Cl·2H2O
C、[Cr(H2O)5Cl]Cl2·H2O D、[Cr(H2O)3Cl3]·3H2O
6.有关晶体的下列说法中正确的是
A、晶体中分子间作用力越大,分子越稳定
B、原子晶体中共价键越强,熔点越高
C、冰熔化时水分子中共价键发生断裂
D、氯化钠熔化时离子键未被破坏
5.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是
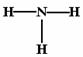
A、一个D2O分子所含的中子数为8 B、NH3的结构式为
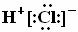 C、HCl的电子式为
C、HCl的电子式为
D、热稳定性:H2S>HF
4.下列分子互为等电子体的是
A、H2O和NH3 B、N2和CO C、SiO2和O3 D、NO2和CO2
3.下列分子中中心原子的杂化轨道类型与其他三个都不一样的是
A、HCN B、CO2 C、BeCl2 D、PCl3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com