
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
ЎЎ |
||||
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|||||
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
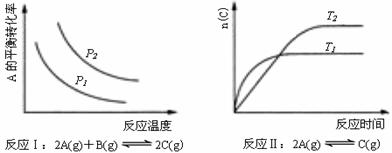
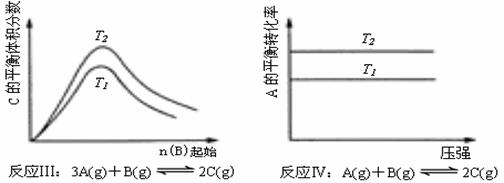
25ЎўДі»ҜС§ҝЖСРРЎЧйСРҫҝФЪЖдЛыМхјюІ»ұдКұЈ¬ёДұдДіТ»Мхјю¶Ф»ҜС§ЖҪәвөДУ°ПмЈ¬өГөҪИзПВұд»Ҝ№жВЙ(НјЦРPұнКҫС№ЗҝЈ¬TұнКҫОВ¶ИЈ¬nұнКҫОпЦКөДБҝ)Јә
 ЎЎ
ЎЎ
ёщҫЭТФЙП№жВЙЕР¶ПЈ¬ПВБРҪбВЫХэИ·өДКЗЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ )
AЈ®·ҙУҰўсЈәЎчHЈҫ0Ј¬P2ЈҫP1ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
BЈ®·ҙУҰўтЈәЎчHЈј0Ј¬T1ЈҫT2
CЈ®·ҙУҰўуЈәЎчHЈҫ0Ј¬T2ЈҫT1Ј»»тЎчHЈј0Ј¬T2ЈјT1
DЈ®·ҙУҰўфЈәЎчHЈј0Ј¬T2ЈҫT1
ЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎөЪўтҫн(·ЗСЎФсМвЎЎ №І55·Ц)
24Ўў әПіЙ°ұ№ӨТө¶Ф№ъГсҫӯјГәНЙз»б·ўХ№ҫЯУРЦШТӘөДТвТеЎЈ№юІ®·ЁәПіЙ°ұРиТӘФЪ20Јӯ50MPaөДёЯС№әН500ЎжөДёЯОВПВЈ¬ІўУГМъЧчОӘҙЯ»ҜјБЈ¬°ұөДЧӘ»ҜВКОӘ10%Јӯ15%ЎЈЧоҪьГА№ъ¶нАХёФҙуС§өД»ҜС§јТК№УГБЛТ»ЦЦГыОӘtransЈӯFe(DMeOPrPE)2өДҙЯ»ҜјБЈ¬ФЪіЈОВПВәПіЙіц°ұЈ¬·ҙУҰ·ҪіМКҪҝЙұнКҫОӘN2+3H2Ўъ2NH3Ј¬УР№ШЛө·ЁХэИ·өДКЗ
AЈ®№юІ®·ЁәПіЙ°ұКЗОьИИ·ҙУҰЈ¬РВ·ЁәПіЙ°ұКЗ·ЕИИ·ҙУҰ
BЈ®РВ·ЁәПіЙәН№юІ®·ЁПаұИІ»РиТӘФЪёЯОВМхјюПВЈ¬ҝЙҪЪФјҙуБҝДЬФҙЈ¬ҫЯУР·ўХ№З°ҫ°
CЈ®РВ·ЁәПіЙДЬФЪіЈОВПВҪшРРКЗТтОӘІ»РиТӘ¶ПБС»ҜС§јь
DЈ®РВөДҙЯ»ҜјБҪөөНБЛ·ҙУҰЛщРиТӘөДДЬБҝЈ¬МбёЯБЛ»о»Ҝ·ЦЧУ°Щ·ЦКэ
23ЎўФЪБҪёцМе»эПаН¬өДГЬұХИЭЖчAЎўBЈ¬ФЪAЦРідИлSO2әНO2ёч1molЈ¬ФЪBЦРідИл
SO2әНO2ёч2 molЈ¬јУИИөҪПаН¬ОВ¶ИЈ¬УРИзПВ·ҙУҰ2SO2(g)+
O2(g)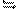 2SO3(g)Ј¬¶ФҙЛ·ҙУҰІ»ХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ ) AЈ®·ҙУҰЛЩВКBЈҫAЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
BЈ®SO2өДЧӘ»ҜВКBЈҫA
2SO3(g)Ј¬¶ФҙЛ·ҙУҰІ»ХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ ) AЈ®·ҙУҰЛЩВКBЈҫAЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
BЈ®SO2өДЧӘ»ҜВКBЈҫA
CЈ®ЖҪәвКұёчЧй·Цә¬БҝB = AЎЎЎЎЎЎЎЎЎЎ DЈ®ЖҪәвКұИЭЖчөДС№ЗҝBЈҫA
22ЎўУГөзҪвЦКИЬТәОӘЗвСх»ҜјШЛ®ИЬТәөДЗвСхИјБПөзіШөзҪвұҘәНМјЛбДЖИЬТәТ»¶ОКұјдЈ¬јЩЙиөзҪвКұОВ¶ИІ»ұдЗТУГ¶иРФөзј«Ј¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ®өұөзіШёәј«ПыәДmgЖшМеКұЈ¬өзҪвіШСфј«Н¬КұУРmgЖшМеЙъіЙ
BЈ®өзіШөДХэј«·ҙУҰКҪОӘЈәO2 + 2H2O + 4e- = 4OH-
CЈ®өзҪвәуc(Na2CO3)І»ұдЈ¬ЗТИЬТәЦРУРҫ§МеОціц
DЈ®өзіШЦРc(KOH)І»ұдЈ»өзіШЦРИЬТәpHұдҙу
21ЎўМе»эПаН¬өДјЧЎўТТБҪёцИЭЖчЦР·Цұр¶јідУРөИОпЦКөДБҝөДSO2әНO2Ј¬ФЪПаН¬ОВ¶ИПВ·ўЙъ·ҙУҰІўҙпөҪЖҪәвЈә2SO2(g) + O2(g)  2SO3(g)ФЪХвёц№эіМЦРјЧИЭЖчұЈіЦМе»эІ»ұдЈ¬ТТИЭЖчұЈіЦС№ЗҝІ»ұдЈ¬ИфјЧИЭЖчЦРSO2өДЧӘ»ҜВКОӘp%Ј¬ФтТТИЭЖчЦРSO2өДЧӘ»ҜВКЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ AЈ®өИУЪp%ЎЎЎЎЎЎЎЎ BЈ®ҙуУЪp%ЎЎЎЎЎЎ CЈ®РЎУЪp%ЎЎЎЎ DЈ®ОЮ·ЁИ·¶Ё
2SO3(g)ФЪХвёц№эіМЦРјЧИЭЖчұЈіЦМе»эІ»ұдЈ¬ТТИЭЖчұЈіЦС№ЗҝІ»ұдЈ¬ИфјЧИЭЖчЦРSO2өДЧӘ»ҜВКОӘp%Ј¬ФтТТИЭЖчЦРSO2өДЧӘ»ҜВКЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ AЈ®өИУЪp%ЎЎЎЎЎЎЎЎ BЈ®ҙуУЪp%ЎЎЎЎЎЎ CЈ®РЎУЪp%ЎЎЎЎ DЈ®ОЮ·ЁИ·¶Ё
20ЎўФЪГЬұХИЭЖчЦРҪшРРПВБР·ҙУҰЈәM(g)+N(g)
 R(g)+2LҙЛ·ҙУҰ·ыәППВБРНјПу(R%ОӘR
R(g)+2LҙЛ·ҙУҰ·ыәППВБРНјПу(R%ОӘR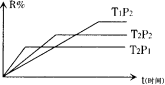 ФЪЖҪәв»мәПОпЦРөДМе»э·ЦКэ)Ј¬ФтёГ·ҙУҰКЗЈәЎЎЎЎЎЎЎЎЎЎ
ФЪЖҪәв»мәПОпЦРөДМе»э·ЦКэ)Ј¬ФтёГ·ҙУҰКЗЈәЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎ AЈ®Хэ·ҙУҰКЗОьИИ·ҙУҰЈ¬LКЗЖшМе
BЈ®Хэ·ҙУҰКЗ·ЕИИ·ҙУҰЈ¬LКЗЖшМеЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎ CЈ®Хэ·ҙУҰКЗОьИИ·ҙУҰЈ¬LКЗ№ММе
DЈ®Хэ·ҙУҰКЗ·ЕИИ·ҙУҰЈ¬LКЗ№ММе»тТәМе
19ЎўУГ¶иРФөзј«өзҪвЈ¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ®өзҪвПЎБтЛбИЬТәЈ¬КөЦКЙПКЗөзҪвЛ®Ј¬№КИЬТәp HІ»ұд
BЈ®өзҪвПЎЗвСх»ҜДЖИЬТәЈ¬ТӘПыәДOHЈӯЈ¬№КИЬТәpHјхРЎ
CЈ®өзҪвПхЛбТшИЬТәТ»¶ОКұјдәуЈ¬ҝЙјУИлСх»ҜТшЈ¬К№ИЬТә»ЦёҙөҪФӯЕЁ¶И
DЈ®өзҪвВИ»ҜНӯИЬТәЈ¬ФЪТхј«ЙПәНСфј«ЙПОціцІъОпөДОпЦКөДБҝЦ®ұИОӘ1:1
18ЎўФЪТ»¶ЁОВ¶ИПВЈ¬Птa LГЬұХИЭЖчЦРјУИл1mol XЖшМеәН2 mol YЖшМеЈ¬·ўЙъИзПВ·ҙУҰЈә
X(g)+2Y(g)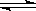 2Z(g) ҙЛ·ҙУҰҙпөҪЖҪәвөДұкЦҫКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(ЎЎЎЎЎЎ
)
2Z(g) ҙЛ·ҙУҰҙпөҪЖҪәвөДұкЦҫКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(ЎЎЎЎЎЎ
)
A.ИЭЖчДЪС№ЗҝІ»ЛжКұјдұд»ҜЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B.ИЭЖчДЪёчОпЦКөДЕЁ¶ИІ»ЛжКұјдұд»Ҝ
C.ИЭЖчДЪXЎўYЎўZөДЕЁ¶ИЦ®ұИОӘ1©U2©U2ЎЎ D.өҘО»КұјдПыәД0.1mol XН¬КұЙъіЙ0.2mol Z
17ЎўПВБРКВКөІ»ДЬУГАХПДМШБРФӯАнҪвКНөДКЗ
AЈ®ҙтҝӘұщХтЖЎҫЖЈ¬ІъЙъҙуБҝөДЕЭДӯ
BЈ®КөСйКТҝЙТФУГЕЕұҘәНКіСОЛ®өД·Ҫ·ЁКХјҜВИЖш
CЈ®Ҫ«Нӯ·ЫәНРҝ·Ы»мәПәу·ЕИлПЎБтЛбЦРЈ¬ІъЙъЖшМеөДЛЩВКұИІ»јУНӯ·ЫКұөДҝм
DЈ®ЦЖБтЛбКұ№ӨТөЙПНЁИл№эБҝөДҝХЖшТФМбёЯ¶юСх»ҜБтөДЧӘ»ҜВК
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com