
题目列表(包括答案和解析)
14、下列操作中错误的是 ( A )
A. 除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯
B. 除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C. 除去CO2中的少量SO2;通过盛有饱和NaHCO3溶液的洗气瓶
D. 提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,取出有机层再分离
13、巴豆酸的结构简式为CH3-CH=CH-COOH,现有: ①氯化氢 ②溴 ③纯碱溶液 ④2-丙醇 ⑤酸化的高锰酸钾溶液。试根据其结构特点判断在一定条件下能与巴豆酸反应的物质组合 ( D)
A. ②④⑤ B. ①③④ C. ①②③④ D. ①②③④⑤
12、只用水就能鉴别的一组物质是 ( A )
A、苯、醋酸、四氯化碳 B、溴乙烷、醋酸、乙醇
C、乙醇、甘油、硝基苯 D、苯酚、甘油、乙二醇
11、下列有机物分子中,所有的原子不可能处于同一平面的是 ( A )
A、CH2=CH-CH3 B、CH2=CH-CH=CH2
C、
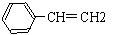 D、CH
D、CH C-CH=CH2
C-CH=CH2
10.下列物质中,与乙醇互为同系物的是 ( B )
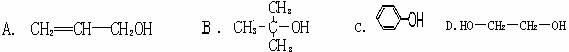
9.下列有机物中沸点最高的是 ( C )
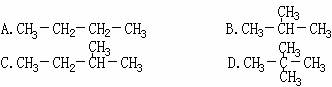
8.下列有关氟氯代烷的说法中,不正确的是 ( B )
A.氟氯代烷是一类含氟和氯的卤代烃 B.氟氯代烷化学性质稳定,有毒
C.氟氯代烷大多无色、无臭、无毒
D.在平流层中,氟氯代烷在紫外线照射下分解产生的氯原子可引发臭气层损耗。
1. 化学平衡中的三大假设思想
在中学化学中,化学平衡问题多局限于定性的阐述,很少有定量的分析。因此,有关化学平衡问题的处理主要是“定性”和“半定量”法,对于近几年高考试题,这种方法主要应用三大假设思想--极端假设、等效假设、过程假设。下面分别谈谈三大假设思想。
第一种,极端假设
化学平衡研究的对象是不能完全进行的反应。极端假设就是把研究的对象或过程假设到能够完全进行的理想的极限情况,使因果关系变得非常明显,从而得出正确的结论。
第二种,等效假设
化学平衡的特点之一是“同”即条件不变时,无论反应是从正反应开始,还是从逆反应开始,还是从既有反应物又有生成物开始,均可以达到同一平衡状态。等效假设就是通过假设能够达到与原平衡起始物质的浓度(或物质的量),相同的条件,均可达到同一平衡状态的方法。
第三种,过程假设
化学平衡的移动是根据勒沙特列原理来进行判断的。但对于一些较为复杂的、抽象的过程往往难以得出结论,如果将其假设为若干个简单的具体的过程,会使问题变得简捷明了,从而得以解决,这种假设叫过程假设。
(参考《中学化学》 陕西,贺种生《化学平衡中的三种假设思想》)
(三)如果用一种反应物和一种生成物表示正逆反应速率时也可以确定平衡状态。应指出的是:(1)两种物质的速率同时都为消耗速率或同时都为生成速率;(2)二者的速率之比等于化学方程式中两种物质的化学计量数之比,此状态即为平衡状态。
例:在合成氨反应中,下列说法可以确定反应达到化学平衡状态的是( )
A. 当有1 mol N≡N键断裂的同时,有3 mol H-H键断裂。
B. 当有1 mol N≡N键断裂的同时,有6 mol N-H键形成。
C. 当有1 mol N≡N键断裂的同时,有6 mol H-H键形成。
D. 当有1 mol N≡N键断裂的同时,有6 mol N-H键断裂。
简析:题中四个选项的前半句都相同,A、B选项无论是否达到平衡都有此变化发生,故不能确定反应是否达到平衡;C选项有6 mol的H-H键形成同时应有2 mol N≡N键断裂,故为非平衡状态(向逆向进行);D选项有6 mol N-H键断裂的同时即形成1 mol N≡N,该选项可确定反应处于平衡状态。故应选D。
(参考《中学化学》,黑龙江,辛占国等《用“正、逆反应速率相等”的观点判断化学平衡》)
(二)如果用两种不同反应物(或两种不同生成物)的速率表示正反应速率和逆反应速率时,也可以确定平衡状态。应指出的是:(1)如果用一种反应物的消耗速率表示正反应速率,则必须用另一种反应物的生成速率表示逆反应速率。(2)二者的速率之比等于化学方程式中两种物质的化学计量数之比。此状态即为平衡状态。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com