
题目列表(包括答案和解析)
23.甲同学在某食品包装袋内,发现有一个装有白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放在空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状固体B。请与甲同学一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有__________、__________。
写出白色颗粒状固体A在空气中转变成块状固体B的有关化学反应方程式:_________
________________________。
(2)猜想二:块状固体B溶于水可能有__________现象(填“放热”或“吸热”)。请设计实验方案验证你的这一猜想(至少写出两种方案,如果写出三种正确方案奖励1分)
①________________________________________________________;
②_______________________________________________________;
③______________________________________________________。
(3)取适量块状固体B加入盛有一定量水的试管中,振荡、静置、过滤,得到少量白色固体C。就白色固体C的成分,甲同学与乙同学进行讨论,一起猜想。甲同学认为,白色固体C可能是氢氧化钙;乙同学认为,白色固体C可能是碳酸钙;你认为,白色固体C,还可能是_________________________。
请设计一个实验验证你的猜想(填写下表):
|
方
案 |
现象和结论 |
|
|
|
22.小明同学在学习酸的性质时,他用大小、外形均相同的铝片分别和H+浓度相同的稀盐酸、稀硫酸反应。他意外地发现:铝片与稀盐酸反应放出气泡的速度明显快于与稀硫酸反应放出气泡的速度。是什么原因导致了反应现象的差异呢?小明从微观角度分析得出,H+浓度相同的盐酸、硫酸中,只是所含_____________不同。
小时提出了如下猜想:
①Cl-能促进铝和酸的反应,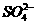 对反应无影响;
对反应无影响;
②Cl-对反应无影响,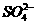 能抑制铝和酸的反应;
能抑制铝和酸的反应;
③Cl-能促进铝和酸的反应,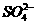 能抑制铝和酸的反应。
能抑制铝和酸的反应。
他进行了如下实验探究:
|
组别 |
相同的铝片 |
H+浓度 相同的酸 |
反应片刻后添加 某种试剂(少量) |
添加试剂后的反应现象 |
结 论 |
|
1 |
1g铝片 |
5mL |
Na2SO4 |
无明显变化 |
_____和_____离子对反应无影响 |
|
2 |
1g铝片 |
5mL |
NaCl |
明显加快 |
_____离子对反应有促进作用 |
针对上述探究过程回答下列问题:
(1)请你将表格中的空格补充完整。
(2)上述猜想____________是成立的。
(3)若将第2组实验中添加的试剂NaCl改为HCl气体,能否完成探究任务?请说明原因。
21. 小远通过查阅资料知道了牙膏的主要成分。他将一定比例的碳酸钙粉末和食盐倒入小烧杯中,然后加入适量甘油(保湿剂)、甜味剂和香精等,搅拌均匀后制得牙膏。
(1)牙膏是___________________ (填“纯净物”和“混合物”)
(2)小远测定自制牙膏及其他清洁用品的pH,记录如下:
|
物质 |
自制牙膏 |
洁厕灵 |
油污净 |
|
pH |
S |
2 |
12 |
自制牙膏显___________(填“酸性”、“碱性”或“中性”),洁厕灵可使紫色石蕊试液变_____。
(3)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果。这种碳酸钙是将二氧化碳通入石灰浆制得的。请写出以石灰石和水为原料制取这种碳酸钙的化学方程式。
__________________________________________________________________________
20. 六朝古都南京的一些古代建筑保存完好,这与所用的建筑材料有关。该小组从某古代建筑维修现场搜集了一些旧墙灰进行研究。取12.0g旧墙灰(主要成分是碳酸钙)放入烧杯中,并加入足量稀盐酸(假设其他也杂质不参加反应,不考虑H2O、HCl逸出)。反应开始时,烧杯及所盛物质的总质量为300.0g。实验数据记录如下:
|
反应时间/min |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
|
烧杯及所盛物 质总质量/g |
300.0 |
299.0 |
298.0 |
297.2 |
296.5 |
296.0 |
295.7 |
295.6 |
M |
295.6 |
 (1)该小组因故没有记录反应时间为16min时的数据M。你由表中数据推测,M=______g;
(1)该小组因故没有记录反应时间为16min时的数据M。你由表中数据推测,M=______g;
(2)反应生成CO2的总质量为_____________g;
(3)根据实验数据,在右边的坐标纸上绘制生成
CO2质量与反应时间关系的曲线。前3min生成
CO2的质量为___________g;
(4)该旧墙灰中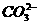 离子的质量分数为______。
离子的质量分数为______。
19. 全世界每年因生锈而损失的钢铁,约占世界钢铁年产量的
全世界每年因生锈而损失的钢铁,约占世界钢铁年产量的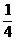 ,某同
,某同
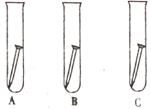
学想弄清楚铁生锈是否必须同时有空气和水,他将干净的铁钉放入A、
B、C三支试管中进行研究。问题:
(1)在如图的每支试管中画出并标明所需的物质和用品。
(2)一周后,编号为______的试管中铁钉最易生锈。
18. 钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注。某化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究。提出假设:a.Ti的金属活动性比Mg 强; b.Ti的金属活动性介于Mg和Ag之间。
查阅资料:在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强。
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象。
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_______(填序号)。
①除去氧化膜,利于直接反应 ②使反应的金属温度相同,易反应 ③使表面光亮,易观察现象
|
金属 |
Ti |
Mg |
Ab |
|
实验现象 |
产生气泡速度缓慢 |
产生气泡速度快 |
无任何现象 |
(2)根据下表中的实验现象填空:
结论:原假设中__________不正确(填“a”、“b”或“ab”),理由是___________;三种金属的活动性由强到弱的顺序为______________________________。
(3)上述实验设计中,如果所用盐酸的溶质质量分数不同,是否一定能够得出正确的结论?________(填“是”或“否”),理由是______________。
17.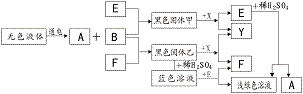 右图为一些常见物质间互相转化的关系图(有些反应条件已省略):已知高温下CO能与多种金属氧化物反应生成相应的金属和CO2。下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。
右图为一些常见物质间互相转化的关系图(有些反应条件已省略):已知高温下CO能与多种金属氧化物反应生成相应的金属和CO2。下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。
(1)根据上图判断B的化学式为___________;Y的化学式为______________。
(2)写出蓝色溶液与E发生的化学方程式_________________________________________。
(3)X除了与黑色固体甲、乙反应外,请再举一例,说明X还能发生化合反应,写出反应的化学方程式______________________________________________________。
16. 把黄豆大小的一小块金属钠投入到盛有水的烧杯中,钠很快熔化成一个银白色的小球,浮在水面上四处游动并发出“嘶嘶”的响声,其化学方程式为2Na+2H2O 2NaOH+H2↑。若将同样大小的金属钠投入到盛有硫酸铜的烧杯中,除发生钠与水的反应外,还可能发生的反应是______________________________(写出化学方程式),并推断可能观察到的现象:___________。
15. 在10-9-10-7m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。如纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是 ( )
A. 纳米铜属于化合物
B.纳米铜颗粒比普通铜更易与氧气发生反应
C.纳米铜与普通铜所含铜原子的种类不同
D. 纳米铜无需密封保存
14.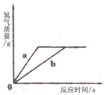 用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如上图所示。则下列说法不正确的是 ( )
用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如上图所示。则下列说法不正确的是 ( )
A. 曲线a、b分别表示锌、铁的反应情况
B. 盐酸均反应完,锌、铁有剩余
C. 盐酸均反应完,锌恰好完全反应,铁有剩余
D. 锌铁都反应完,盐酸有剩
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com