
题目列表(包括答案和解析)
3、可逆反应达到平衡的重要特征是
A、反应停止了 B、正逆反应的速率均为零
C、正逆反应都还在继续进行 D、正逆反应的速率相等
答案:D
2、在一定温度下,可逆反应A(g)+3B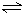 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是
A、C生成的速率与C分解的速率相等
B、A、B、C的浓度不再变化
C、单位时间内,生成n mol A,同时生成3n mol B
D、A、B、C的分子数之比为1:3:2
分析:在一定温度下,判断某可逆反应达到平衡的标志是:(1)V正=V逆
(2)各物质的物质的量不变;(3)每一种物质的浓度不变等。
答案:A B
|
可能的情况举例 |
是否能判断已达平衡 |
|
|
1、混合物体系中各成分的含量 |
①各物质的物质的量或各物质的量的分数一定 |
平衡 |
|
②各物质的质量或各物质的质量分数一定 |
平衡 |
|
|
③各气体的体积或体积分数一定 |
平衡 |
|
|
④总体积、总压强、总物质的量一定 |
无法判断 |
|
|
2、正、逆反应速率的关系 |
①单位时间内消耗了m mol A,同时生成m mol A |
平衡 |
|
②单位时间内消耗了n mol B,同时消耗了p mol C |
平衡 |
|
|
③v(A):v(B):v(C):v(D)=m:n:p:q |
无法判断 |
|
|
④单位时间内生成n mol B,同时消耗q mol D |
无法判断 |
|
|
3、压强 |
①其他条件不变,m+n≠p+q时,总压力一定 |
平衡 |
|
②其他条件不变,m+n=p+q时,总压力一定 |
无法判断 |
|
|
4、平均相对分子质量M |
①当m+n≠p+q时,M一定 |
平衡 |
|
②当m+n=p+q时,M一定 |
无法判断 |
|
|
5、温度 |
其他条件一定时,体系温度一定 |
平衡 |
|
6、体系密度 |
其他条件一定时,密度一定 |
无法判断 |
|
7、其他 |
组成成分有颜色时,体系颜色不再变化 |
平衡 |
|
典例剖析 |
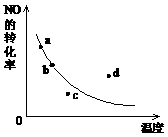 [例1] 右图中的曲线是表示其他条件一定时,2NO+O2
[例1] 右图中的曲线是表示其他条件一定时,2NO+O2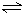 2NO2 △H<0,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 △H<0,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
A、a点 B、b点
C、c点 D、d点
分析:此题为温度--转化率曲线,由于a点、b点均在平衡线上,表示a点与b点均达到平衡状态。
c点时,若温度不变,NO的转化率将增大,说明反应没达到平衡,且反应向正反应方向进行,即v(正)>v(逆),符合题目要求。
d点时,若温度不变,NO的转化率将减小,说明反应没达到平衡,且反应向逆反应方向进行,即v(正)<v(逆),不符合题目要求。
答案:C
拓展:本题是反应物的转化率与平衡线的关系问题,让学生认识面上的不同位置的点与平衡线的关系。解答图象题的方法与思路是:(1)看懂图像:一看面(即看清横坐标和纵坐标),二看线(即看线的走向、变化的趋势),三看点(即看线是否通过原点,两条线的交点及线的拐点),四看要不要作辅助线(如等温线、等压线),五看定量图像中有关量的多少。(2)联想规律:即联想外界条件对化学反应速率和化学平衡的影响规律,且熟练准确。(3)作出判断:依题意仔细分析作出正确判断。
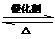 [例2] 在一定温度下,把2 mol SO2和1 mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O2 2SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同。请填写下列空白:
[例2] 在一定温度下,把2 mol SO2和1 mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O2 2SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同。请填写下列空白:
(1)若a=0,b=0,则c=________。
(2)若a=0.5,b=________和c=________。
(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c):_____________。
分析:本题是对可逆反应和化学平衡状态的理解以及利用题给信息将化学问题以及内在规律抽象为数学问题,利用数学工具解决化学问题的思维能力的综合考查。
对于平衡状态的建立,只与条件相关,即与温度、压强(或容器的容积)、反应物或生成物的起始量的相对关系有关,而与反应进行的方向无关。因此,对于该条件下的反应,初始态是2 mol SO2和1 mol O2的混合物,或是2 mol纯净的SO3,两者是等价的,最终达到的平衡状态完全相同。因此(1)中答案应为c=2。而(2)中初始态包含了三种气态物质,此时需要进行思维转换,将初始物质的加入量转换为相当于a=2,b=1,就可以达到题设的平衡状态。现在a=0.5,则b=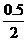 =0.25,此时与题干所设初始态的差是Δa=2-0.5=1.5,Δb=1-0.25=0.75,由此SO3的初始入加量c必须转化为等效于a=1.5和b=0.75的量,根据该反应方程式系数比推断知c=1.5。(3)中要求将具体问题抽象为普通规律,此时必须把握“把所有初始物都转换为反应物,则必须相当于2 mol SO2和1 mol O2的混合物,把所有的初始物转换为生成物,则必须相当于2 mol纯净的SO3。才能得出正确结论:必须同时满足:a+c=2和2b+c=2两个关系式。
=0.25,此时与题干所设初始态的差是Δa=2-0.5=1.5,Δb=1-0.25=0.75,由此SO3的初始入加量c必须转化为等效于a=1.5和b=0.75的量,根据该反应方程式系数比推断知c=1.5。(3)中要求将具体问题抽象为普通规律,此时必须把握“把所有初始物都转换为反应物,则必须相当于2 mol SO2和1 mol O2的混合物,把所有的初始物转换为生成物,则必须相当于2 mol纯净的SO3。才能得出正确结论:必须同时满足:a+c=2和2b+c=2两个关系式。
答案:(1)c=2 (2)b=0.25,c=1.5 (3)a+c=2,2b+c=2
拓展:化学平衡的建立与途径无关,只要可逆反应在相同状况下,无论从正反应或从逆反应开始,都可以建立相同的平衡状态,平衡时各物质的浓度也不因反应从哪边开始而变化。此类题也要注意两类方程式和两种条件。
(I)H2+I2(g)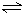 2HI(△v=0)
2HI(△v=0)
(Ⅱ)2SO2+O2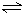 2SO3(△v≠0)
2SO3(△v≠0)
条件一:等温等容
条件二:等温等压
例如在一个容积固定的密闭容器中,加入2 mol A和1 mol B,发生反应
2A(g)+B(g)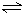 3C(g)+D(g),反应达到平衡时,若生成物C的浓度为a mol·L-1,则在容积和温度不变时,加入3 mol C和1 mol D或加入1 mol A、0.5 mol B、1.5 mol C、0.5 mol D,达到平衡后,生成C的浓度仍为a mol·L-1,但若温度不变,而容积为原情况的2倍,加入4 mol A和2 mol B达到平衡时,C的浓度仍为a mol·L-1。
3C(g)+D(g),反应达到平衡时,若生成物C的浓度为a mol·L-1,则在容积和温度不变时,加入3 mol C和1 mol D或加入1 mol A、0.5 mol B、1.5 mol C、0.5 mol D,达到平衡后,生成C的浓度仍为a mol·L-1,但若温度不变,而容积为原情况的2倍,加入4 mol A和2 mol B达到平衡时,C的浓度仍为a mol·L-1。
|
素能培养 |
A组
1、下列哪种说法可以证明反应:N2+3H2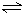 2NH3已达到平衡状态
2NH3已达到平衡状态
A、1个N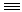 N键断裂的同时,有3个H-H键形成
N键断裂的同时,有3个H-H键形成
B、1个N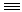 N键断裂的同时,有3个H-H键断裂
N键断裂的同时,有3个H-H键断裂
C、1个N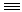 N键断裂的同时,有6个N-H键断裂
N键断裂的同时,有6个N-H键断裂
D、1个N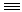 N键断裂的同时,有6个N-H键形成
N键断裂的同时,有6个N-H键形成
答案:A C
2、化学平衡状态
(1)定义:指在一定条件下的可逆反应,正反应和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态。
(2)特征:
① 逆:可逆反应
② 等:v(正)=v(逆)
③ 动:动态平衡v(正)=v(逆)≠0
④ 定:平衡状态时反应混合物中各组分的浓度保持不变
⑤ 变:当浓度、温度、压强等条件改变时,化学平衡即发生移动
(3)特点:
化学平衡的建立与建立的途径无关
(4)达到平衡的标志:以mA(g)+nB(g)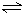 pC(g)为例
pC(g)为例
直接标志:
①速率关系:正反应速率与逆反应速率相等,A消耗速率与A的生成速率相等,A的消耗速率与C的消耗速率之比等于m:p,B生成速率与C的生成速率之比等于n:p。
②各物质的百分含量保持不变。
间接标志:
① 混合气体的总压强、总体积、总物质的量不随时间的改变而改变。(注:m+n≠p)
② 各物质的浓度不随时间的改变而改变。
③ 各物质的物质的量不随时间的改变而改变。
④ 各气体的体积、各气体的分压不随时间的改变而改变。
1、化学平衡的建立
 以CO+H2O(g)
CO2+H2反应为例。
以CO+H2O(g)
CO2+H2反应为例。
在一定条件下,将0.01 mol CO和0.01 mol H2O(g)通入1 L密闭容器中,开始反应:
(1)反应刚开始时:
反应物的浓度 最大 ,正反应速率 最大 。
生成物的浓度为 零 ,逆反应速率为 零 。
(2)反应进行中:
 反应物的浓度逐渐减小,正反应速率逐渐减小。
反应物的浓度逐渐减小,正反应速率逐渐减小。
生成物的浓度逐渐增大,逆反应速率逐渐增大。
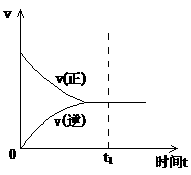
(3)肯定最终有一时刻,正反应速率与逆反应速率相等,此时,反应物的浓度不再变化,生成物的浓度也不再变化。
正反应速率和逆反应速率随时间的变化关系如图所示。
15.根据下列有机物转化关系回答问题:
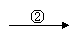

乙醇 乙醛 乙酸 乙酸乙酯
(1)写出反应①的化学方程式
(2)写出反应③的反应类型
(3)写出乙酸乙酯的结构简式
14.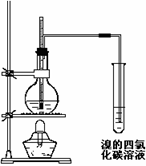 实验室利用加热酒精和浓硫酸的混合液来制取乙烯,下图是乙烯制取和性质实验装置图。试回答下列问题:
实验室利用加热酒精和浓硫酸的混合液来制取乙烯,下图是乙烯制取和性质实验装置图。试回答下列问题:
(1)写出实验室制乙烯的化学方程式
(2)烧瓶内混合液中,放入几片碎瓷片,其目的是
(3)乙烯气体通过溴的四氯化碳溶液的实验现象是
13.写出下列反应的化学方程式:
(1)苯酚溶液中滴加NaOH溶液
(2)苯和浓硝酸,浓硫酸混合溶液共热至55℃-60℃
12.醋酸乙酯在KOH溶液催化下水解,得到的产物是
A.乙酸钾 B.甲醇 C.甲酸 D.乙酸
请将选择题答案按题目顺序填入下列方框中:
11.下列各组混合物中,不能混溶的是
A.乙醛和乙醇 B.苯和水 C.酒精和水 D.乙醛和水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com