
题目列表(包括答案和解析)
10、在一固定容积的密闭容器中,加入4 L
X(g)和6 L Y(g),发生如下反应:X(g)+nY(g)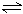 2R(g)+W(g)反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为
2R(g)+W(g)反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为
A、4 B、3 C、2 D、1
分析: x(g) + ny(g) 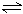 2k(g) +
w(g)
2k(g) +
w(g)
起始 4L 6L
转化 4 L×25% 4 L×25%·n
而y转化量为6 L×50%,所以4 L×25%n=6 L×50%;n=3
答案:B
9、在一个密闭容器中发生如下反应:2SO2(g)+O2(g)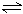 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2 mol·L-1,0.2 mol·L-1,0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2 mol·L-1,0.2 mol·L-1,0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
A、c(SO3)=0.4 mol·L-1
B、c(SO2)=c(SO3)=0.15 mol·L-1
C、c(SO2)=0.25 mol·L-1
D、c(SO2)+c(SO3)=0.4 mol·L-1
分析:2SO2(g)+O2(g)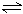 2SO3(g)
2SO3(g)
反应过程中某一时刻C(SO2)=0.2 mol·L-1,C(O2)=0.2 mol·L-1
C(SO3)=0.2 mol·L-1
若SO2全部转化为SO3,C(SO3)=0.2 mol·L-1+0.2 mol·L-1=0.4 mol·L-1,由于是可逆反应,不可能全部转化,所以A选项错,在题述某一时刻之后,无论平衡怎样移,都不能出现C(SO2):C(SO3)=0.15 mol·L-1这种情形,抓住S元素守恒,D选项恒成立,C选项可以出现。
答案:C D
8、在一密闭容器内使1 L NO2分解成NO和O2,达到平衡时,气体的总体积变为1.2 L,则下列说法错误的是
A、NO2的分解率为40%
B、达到平衡时,NO2、NO、O2的物质的量之比是3:2:1
C、NO2的分解率是60%
D、达到平衡时,NO2、NO、O2的质量之比是3:2:1
分析:设NO2的分解率为x
2NO2(g)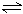 2NO(g)+O2(g)
2NO(g)+O2(g)
起始 1
分解 1·x 1·x 
平衡 1-x
x

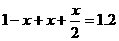 x=40%
x=40%
n(NO2):n(NO):n(O2)
=(1-x):x: =(1-40%):40%:20%=3:2:1
=(1-40%):40%:20%=3:2:1
答案:C D
7、将固体NH4I置于密闭容器中,在某浓度下发生下列反应:NH4I(s)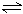 NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g)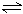 H2(g)+I2(g)。当反应达到平衡时,[H2]=0.5 mol·L-1,[HI]=4 mol·L-1,则NH3的浓度的为
H2(g)+I2(g)。当反应达到平衡时,[H2]=0.5 mol·L-1,[HI]=4 mol·L-1,则NH3的浓度的为
A、3.5 mol·L-1 B、4 mol·L-1
C、4.5 mol·L-1 D、5 mol·L-1
分析:[H2]=0.5 mol·L-1分解的[HI]=1 mol·L-1,所以[NH3]=[HI]平+[HI]分=5 mol·L-1。
答案:D
6、在一个固定容积的密闭容器中,加入m mol A和n mol B,发生下列反应:mA(g)+nB(g)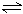 pC(g),平衡时C的浓度为w mol·L-1。若维持容器体积和温度不变,起始时放入a mol A,b mol B,c mol C,要使平衡时C的浓度仍为w mol·L-1,则a、b、c必须满足的关系是
pC(g),平衡时C的浓度为w mol·L-1。若维持容器体积和温度不变,起始时放入a mol A,b mol B,c mol C,要使平衡时C的浓度仍为w mol·L-1,则a、b、c必须满足的关系是
A、a:b:c=m:n:p
B、a:b=m:n: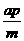 +b=p
+b=p
C、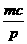 +a=m;
+a=m;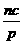 +b=n D、a=
+b=n D、a= ,b=
,b=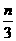 ,c=
,c=
分析:此题是等效平衡问题
mA(g)+nB(g)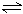 pC(g)
pC(g)
a mol b mol c mol
等效转换: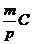
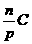
答案:C D
5、加热N2O3时,发生以下两个分解反应:
N2O5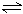 N2O3+O2
N2O3+O2
N2O3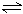 N2O+O2
N2O+O2
在1 L密闭容器中加热4 mol N2O5达到化学平衡时c(O2)为 4.50 mol·L-1,c(N2O3)为1.62 mol·L-1,则该温度下各物质的平衡浓度不正确的是
A、c(N2O5)平=1.44 mol·L-1 B、c(N2O5)平=0.94 mol·L-1
C、c(N2O)平=1.44 mol·L-1 D、c(N2O)平=3.48 mol·L-1
答案:A D
4、对于一定条件下,在密闭容器中已达到平衡状态的可逆反应:NO2+CO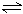 NO+CO2下列说法中不正确的是
NO+CO2下列说法中不正确的是
A、平衡体系中气体总的物质的量等于开始反应时体系中气体总的物质的量
B、从开始反应至达到平衡状态,容器内压强始终保持不变
C、达到平衡时,NO2、CO2、NO、CO的物质的量均相等
D、达到平衡时,NO和CO2的物质的量之和等于NO2和CO的物质的量之和
分析:这是体积不变的反应,因此在体积不变的密闭容器中压强不变,而各物质的物质的量则要受初始加入物质的量及平衡常数的影响。所以C、D错误。
答案CD
3、将2 mol SO2和2 mol SO3气体混合于固定容积的密闭容器中,在一定条件下发生反应:2SO2+O2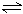 2SO3平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是
2SO3平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是
A、2 mol SO2和1 mol O2
B、4 mol SO2和1 mol O2
C、2 mol SO2、1 mol O2和2 mol SO3
D、3 mol SO2、1 mol O2和1 mol SO3
分析:此题是等效平衡问题
2 mol SO2、2 mol SO3的混合气等效转换,相当于4 mol SO2,1 mol O2,A、B两选项显然不符题意。
答案:C D
2、在一个容积为6 L的密闭容器中,放入3 L X(g)和2 L Y(g),在一定条件下发生反应:4X(g)+nY(g)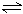 2Q(g)+6R(g),反应达到平衡后,容器内温度不变,混合气体的压强比原来增加了5%,X的浓度减小1/3,则该反应中的n值为
2Q(g)+6R(g),反应达到平衡后,容器内温度不变,混合气体的压强比原来增加了5%,X的浓度减小1/3,则该反应中的n值为
A、3 B、4 C、5 D、6
分析:平衡后x的浓度减小1/3,即反应掉1 L
4x(g)+ny(g)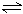 2Q(g)+6R(g)
2Q(g)+6R(g)
起始 3 2
转化 1  0.5 1.5
0.5 1.5
平衡 2  0.5 1.5
0.5 1.5
在恒温恒容下,
 解得:n=3
解得:n=3
答案:A
1、在一定温度下,将2mol SO2和1mol O2充入一定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g)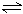 2SO3(g),△H=-197kJ·mol-1。当达到化学平衡时,下列说法中正确的是
2SO3(g),△H=-197kJ·mol-1。当达到化学平衡时,下列说法中正确的是
A、生成SO3 2mol B、放出197kJ热量
C、SO2和SO3共2mol D、含氧元素8mol
分析:此反应是一个可逆反应,反应不可能彻底,因此,A、B两选项错误,根据元素守恒,SO2和SO3其2 mol,O元素6 mol。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com