
题目列表(包括答案和解析)
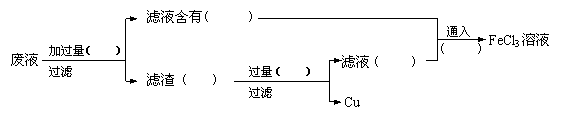
23.电子工业常用30%的溶液腐蚀敷在塑料板上的铜箔,制成印刷电路板,现拟采用以下实验步骤从使用过的腐蚀废液中回收铜,并重新制得纯净的溶液,请在各步骤的括号内填写适当的试剂或生成物的化学式。
22.某无色透明溶液,投入金属铝可放出H2。现有下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-。试判断下列两种情况时,各有哪些离子可存在于此溶液中:
(1)当生成Al3+时,可存在的离子有 ;
(2)当生成AlO2-时,可存在的离子有 。
21.铁粉与足量盐酸反应,离子方程式为 ,将所得溶液分放于二支试管中,第一支加入NaOH溶液,现象是 ,有关反应的化学方程式为 ,第二支中先加入KSCN溶液再通入足量Cl2,现象是 ,有关反应的离子方程式是 。
20.将FeCl2、FeCl3、CuCl2三种溶液及Fe、Cu放入同一容器中,分别在下述情况下,哪些阳离子或金属单质能同时存在(不考虑极少量的H+):
(1)反应后Fe剩余,容器内还可能有 ;
(2)反应后溶液中有较多的Cu2+,容器内还可能有 或 。
19.铁元素位于周期表中 周期 族,是一种重要的过渡元素。在铁的化合物中铁显示正二价的原因是 ,显示正三价的原因是 。
18.铝热剂是 和 的混合物,其反应的方程式为(举例) ,此反应可用于 。
17.铝元素的单质既能与强酸反应、又能与强碱溶液反应,其离子方程式分别为 、 。
16.地壳中含量最多的金属元素和含量最多的非金属元素形成的化合物的化学式为 ,此化合物与盐酸、NaOH溶液可发生化学反应,反应的离子方程式分别为 、 。
15.已知空气-锌电池的电极反应为: 锌片:Zn + 2OH――2e-= ZnO + H2O 石墨:1/2O2+H2O + 2e- = 2OH- 据此判断:锌片是:
A. 负极,并被氧化 B. 负极,并被还原
C. 正极,并被氧化 D. 正极,并被还原
14.有2 mol/L的盐酸和硫酸各100 mL ,分别加入等质量的铁粉,反应结束后,所生成气体的质量比为2∶3,则向盐酸中加入铁粉的质量是( )
A. 11.2 g B. 2.3 g C. 5.6 g D. 8.4 g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com