
题目列表(包括答案和解析)
4.(3分,每空1分) HCl、NO NH3、O2 CO2
3.(2分,每空1分) CH2==CHCH2CH3 CH3CH==CHCH3
2.(2分,每空1分) 铝、铁 钝化
1.(2分,每空1分) 小苏打 黄
第Ⅱ卷(非机读卷 共40分)
12.(6分)请在以下(1)、(2)两小题中任选作一题。
(1)某同学在实验室进行甲、乙、丙、丁4组实验:各取40mL同浓度的盐酸,加入同一种镁铝合金粉末,合金质量和生成气体体积记录如下表。
|
实验序号 |
甲 |
乙 |
丙 |
丁 |
|
合金质量(g) |
0.204 |
0.306 |
0.408 |
0.510 |
|
生成气体体积(mL) (标准状况) |
224 |
336 |
448 |
448 |
请回答:
①盐酸的物质的量浓度为 ;
②乙组合金中镁的质量是 ;
③若在甲组实验后的溶液中加入浓度为0.5mol/L NaOH溶液,使产生的Al(OH)3沉淀恰好溶解,则需NaOH溶液的体积为 。
(2)由H2、C2H2、C2H4组成的1L混合气体在一定条件下发生加成反应后,气体总体积变成xL(气体体积均在标准状况下测定)。请回答:
①当反应后三种气体均无剩余时,x的取值范围是_____________;若x==0.4时,原混合气体H2、C2H2、C2H4的体积比为___________;
②当x==0.6,且反应后混合气体密度为0.714g/L时,原混合气体H2、C2H2、C2H4的体积比为 。
高二化学会考模拟试卷(四)
第Ⅰ卷(机读卷 共60分)
11.(4分)将11.2L氢气和14.2g氯气混合,使其在光照条件下充分反应,并将生成的氯化氢全部溶于水制成250mL溶液。试计算(气体体积均在标准状况下测定):
(1) 哪种反应物有剩余?剩余多少升?生成氯化氢的体积。
(2) 所得溶液的物质的量浓度。
10.(4分)A、B、C、D、E是中学化学中常见的有机物,它们之间的反应关系如下图所示(图中部分反应条件和无机物已经略去):
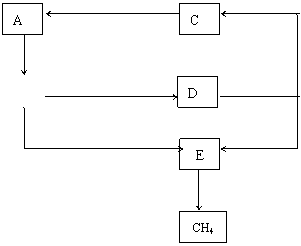
|
浓硫酸,加热
加热
(1)分子式与D相同的酯类物质共有 种;
(2)在生成A的反应过程中,C分子内被破坏的化学键是___________键(填序号);
① O-H ② C-H ③ C-C ④ C-O
(3)为了验证物质A的性质,某同学向2mL 2% 硫酸铜溶液中滴入4-5滴10% NaOH溶液,生成淡蓝色絮状沉淀,然后加入0.5mL A的稀溶液,加热,结果未出现红色的氧化亚铜沉淀。试分析实验失败的原因:___________________________________________ 。
9.(4分)为测定由CO、NH3、CO2、H2组成的混合气体中各成分的体积分数,请用下列装置设计一个简单实验(装置不能重复使用,所用试剂均过量)。
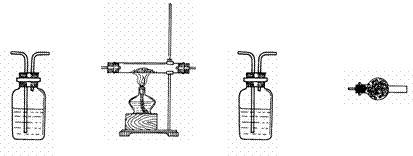 氧化铜
氧化铜


碱石灰
浓硫酸 Ba(OH)2溶液
① ② ③ ④

已知存在下列反应: 2NH3 +3 CuO 3Cu + N2 + 3H2O
请回答:
⑴ 混合气体通过各装置的顺序依次是( )→( ① )→( )→( );
⑵ 写出装置③中有关反应的离子方程式 ;
⑶ 装置③和④的位置不可互换,其原因是 。
8.(3分)某同学欲用12mol/L的浓盐酸配制1mol/L的盐酸250mL。
(1)操作时,必须用到的仪器是 ______________________(填序号)。
①500mL容量瓶 ②250mL容量瓶 ③100mL烧杯 ④50mL量筒 ⑤10mL量筒
(2)操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是 。
(3)用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是_______(填序号)。
①吸出多余液体,使凹液面与刻度线相切 ②小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
③经计算加入一定量的浓盐酸 ④重新配制
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com