
题目列表(包括答案和解析)
15.下列离子方程式正确的是 [ ]。
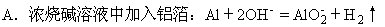
B.氯化铁溶液中加入铁粉:Fe+Fe3+=2Fe2+
C.硫酸铜溶液中加入硫化氢溶液:Cu2++S2-=CuS↓
D.碳酸氢镁溶液中加入足量烧碱溶液:

14.将等物质的量的Mg和Al混合均匀,分成四等份,分别加到下列四种过量的溶液中,充分反应后,放出H2最多的是 [ ]。
A.3 mol/L HCl溶液 B.4 mol/L HNO3溶液
C.8 mol/L NaOH溶液 D.18 mol/L H2SO4溶液
13.向含有①Mg2+,②Fe2+,③NH4+,④Al3+的溶液中,加入过量的NaOH溶液,加热并搅拌,再加入过量盐酸,溶液中减少的阳离子是 。
A.①② B.①④ C.③④ D.②③
12.下列事实能说明醋酸属干弱电解质的县 [ ]。
①中和 10 mL 1 mol/L CH3COOH溶液需要 10 mL1 mol/L NaOH溶液
②物质的量浓度相同时,锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01 mol/L醋酸溶液的pH大于2
④0.1 mol/L CH3COONa溶液显碱性
A.①②③ B.②③④ C.①③④ D.①④
11.某温度下,在固定容积的容器中,可逆反应A(g)+3B(g) 2C(g)达到平衡,此时测得n(A):n(B):n(C)=2:2:1。若保持温度不变,以n(A):n(B):n(C)= 2:2:1的比例向该容器中再充入A、B和C则 [ ]。
2C(g)达到平衡,此时测得n(A):n(B):n(C)=2:2:1。若保持温度不变,以n(A):n(B):n(C)= 2:2:1的比例向该容器中再充入A、B和C则 [ ]。
A.平衡向正反应方向移动 B.平衡向逆反应方向移动
C.平衡不发生移动 D.A的百分含量增大
10.将0.l mol N2O4置于1L密闭烧瓶中,然后将烧瓶放入100℃的恒温槽里,烧瓶内的气体逐渐变为红棕色:N2O4(g)(无色) 2NO2(g)(红棕色)
2NO2(g)(红棕色)
下列结论不能说明上述反应在该条件下已经达到平衡状态的是 [ ]。
A.烧瓶内气体的颜色不变,不再加深
B.N2O4的消耗速率与NO2的生成速率之比为1:2
C.NO2的生成速率与NO2的消耗速率相等 D.NO2的物质的量浓度不变
9.下列化合物中既含有离子键又含有极性共价键的是 [ ]。
A.NaBr B.NH4Cl C.KI D.CaCl2
8.下列分子中,具有极性键的非极性分子是 [ ]。
A.H2O B.NH3 C.CCl4 D.Br2
7.X、Y、Z是周期表中三种相邻的元素,X和Y同周期,Y和Z同主族。这三种元素原子的最外电子层中电子数的总和是17,核内质子数的总和是31,则X、Y、Z三种元素是下列各组中的 [ ]
A.N、O、S B.O、S、P C.O、F、Cl D.C、Si、P
6.在化学上,常用CaH2作为制取氢气的药剂,有关的化学反应方程式为:
CaH2+2H2O=Ca(OH)2+2H2↑在这个反应中,H2O的作用 [ ]
A.是还原剂 B.是氧化剂 C.是溶剂 D.既不是氧化剂,也不是还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com