
题目列表(包括答案和解析)
1、下列物质的水溶液,其pH小于7的是
A.Na2CO3 B.NH4NO3 C.Na2SO4 D.KNO3
25、(14分)在一个容积为500mL的密闭容器中,充入5mol H2和2mol CO,在一定温度,一定压强下,发生如下反应:H2(g)+CO(g) CH3OH(g)
CH3OH(g)
经5min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,求:
⑴以H2的浓度变化表示的该反应的速率?
⑵达平衡时CO的转化率?
⑶平衡混合气体的密度与相同状况下的氢气的密度之比?
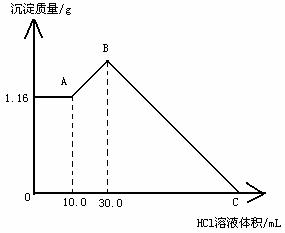
24、(12分)把NaOH、MgCl2、AlCl3、三种固体组成的混合物溶于足量的水后,产生1.16g白色沉淀,再向所得浊液中逐滴加入1.00 mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。试回答:
⑴A点的沉淀物的化学式为
⑵写出A点至B点发生反应的离子方程式
⑶原混合物中MgCl2的质量是 g、
AlCl3的质量为 g、
NaOH的质量为 g
⑷C点HCl溶液的体积为 mL。
22、(10分)某学生用0.1mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
A、移取20ml待测盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B、用标准溶液润洗滴定管2-3次
C、把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D、取KOH标准溶液注入碱式滴定管至刻度0以上2-3厘米
E、调节液面至0或0以下刻度,记下读数
F、把锥形瓶放在滴定管的下面,用标准的KOH溶液滴定至终点并记下滴定管液面的刻度。就此实验完成。
填空:⑴正确操作步骤顺序是(用序号字母填写)
⑵上述B步骤操作的目的是
⑶上述A步骤操作之前,先用待测溶液润洗锥形瓶,则对滴定结果的影响是
⑷判断到达滴定终点的实验现象是:
⑸若称量一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果的影响是 23、(12分)硫酸氢钾溶液显 性( 填“酸”、“碱”或“中”下同),用方程式表示为 ;
碳酸氢钠溶液显 性,用方程式表示为 ;
硫酸铵溶液显 性,用方程式表示为 ;将上述三种溶液混合,现象是 ;
反应的离子方程式为
21、(12分)下面a-e是中学化学实验中常见的几种定量仪器:a、量筒;b、容量瓶;c、滴定管;d、托盘天平;e、温度计
(1)其中标示出仪器使用温度的是 (填写编号);
(2)能够用以精确量取液体体积的是 (填写编号);
(3)由于错误操作,使得到的数据比正确数据偏小的是 (填写编号);
A、用量筒量取一定量的液体时,俯视液面读数
B、中和滴定达终点时俯视滴定管内液面度数
C、使用容量瓶配置溶液时,俯视液面定容后所得溶液的浓度
(4)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为 克。
20、常温下,强酸溶液A和强碱溶液B的pH之和为16,当它们按一定体积比混合时,溶液的pH恰好等于7,则A与B的体积比是 :( )
A 1:10 B 10:1 C 1:100 D 100:1
II卷
19、用标准NaOH溶液滴定未知浓度的盐酸溶液,以测定盐酸的浓度,下列操作使测定结果偏高的是 ( )
A 未知浓度盐酸用滴定管量取,该滴定管用蒸馏水洗涤后未用待测液润洗
B 装待测液的锥形瓶,洗涤后未干就盛入待测液
C 滴完开始时,用俯视法观察碱式滴定管刻度,其余操作正确
D滴定结束后,发现碱式滴定管尖嘴处悬挂一滴碱液
18、在同体积pH=3的H2SO4、HCl、HNO3、CH3COOH溶液中,加入足量锌粉,下列说法正确的是:( )
A H2SO4中放出H2最多
B 醋酸中放出H2最多
C HCl和HNO3放出H2一样多
D HCl比HNO3 放出H2多
17、在硫酸铝、硫酸钾、明矾三种物质的混合溶液中,c(SO42-)=0.2mol/L,向其中加入等体积的0.2mol/LKOH溶液,使生成的白色沉淀又恰好溶解,则原混合溶液中c(K+)为 ( )
A 0.15mol/L B 0.25mol/L
C 0.225mol/L D 0.45mol/L
15、某二元弱酸的酸式盐NaHA溶液,若pH<7,则溶液中各离子的浓度关系不正确的是( )
A c(Na+)> c(HA-)>c(H+)>c(A2-)>c(OH-)
B c(Na+)+C(H+)=c(HA-)+2c(A2-)+c(OH-)
C c(H+)+c(A2-)=c(OH-)+c(H2A)
D c(Na+)=c(HA-)+c(H2A)+c(A2-)
16用某种仪器测量一液体的体积时,平视读数为n mL,仰视读数为x mL,俯视读数为y mL。若x> n> y,则使用的仪器可能是()
A烧杯 B 量筒
C 酸式滴定管 D 容量瓶
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com