
题目列表(包括答案和解析)
13.在N2+3H2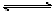 2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,在此时间内用H2表示的平均反应速率为0.45
mol/L·s,则所经历的时间是( )
2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,在此时间内用H2表示的平均反应速率为0.45
mol/L·s,则所经历的时间是( )
(A)0.44s (B)1s (C)1.33s (D)1.2s
12.用3克块状大理石与30毫升3摩/升盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
(a)再加入30毫升3摩/升盐酸 (b)改用30毫升6摩/升盐酸
(c)改用3克粉末状大理石 (d)适当升高温度
( A )(a)(b)(d) ( B )(b)(c)(d) ( C )(a)(c)(d) ( D )(a)(b)(c)
0.(C)01mol/(L·s) (D) 0.03mol/(L·s)
0.(A)1mol/(L·s) (B) 0.3mol/(L·s)
11.在一密闭容器中,盛有N2和H2,它们的起始浓度分别是1.5mol/L和4.5mol/L。一定条件下发生反应生成NH3,10秒钟后测得N2的浓度是1.4mol/L。则H2在10秒钟内的平均反应速率是( )
9.100mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
(A)碳酸钠固体 (B)乙酸钠固体 (C)硫酸钾固体 (D)硫酸铵固体
10.NO与CO都是汽车尾气里有害的物质,它们能缓慢地起反生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
(A) 使用催化剂可以加快反应速率
(B) 其它条件不变,升温反应速率会加快
(C)其它条件不变,加压对反应速率没有影响
(D)外界任何条件怎样改变,均对此化学反应速率无影响
8.反应4NH4+5O2=4NO+6H2O在5升的密闭容器中进行,半分钟后,NO增加了0.3摩,则此反应的反应速度(表示反应物的消耗速度或生成物的生成速度)为
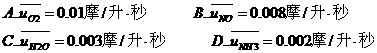
7.已知4NH3+5O2=4NO+6H2O,若反应速度分别用VNH3、VO2、VNO、VH2O(摩/升分)。则正确的关系是
(A)4VNH3/5=VO2 (B)5VO2/6=VH2O (C)2VNH3/3=VH2O (D)4VO2/5=VNO
6.合成氨的反应为3H2+N2=2NH3,其反应速度可以用VH2、VN2、VNH3(摩/升·秒)表示,则正确的关系式是
(A)VH2=VN2=VNH3 (B)VN2=3VH2 (C)VNH3=3VH2/2 (D)VH2=3VN2
5.在一个容积为2L的密闭容器中,发生如下反应:3A+B=2C (A.B.C均为气体)若最初加入的A.B都是4mol,A的平均反应速率为0.12mol/L·s,则10s后容器中的B是
A.2.8mol B.1.6mol C.3.2mol D.3.6mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com