
题目列表(包括答案和解析)
31、(8分)为了测定乙醇的结构式,有人设计了用无水酒精与钠反应的实验装置和测定氢气体积的装置进行实验。可供选用的实验仪器如右图所示。
 请回答以下问题:
请回答以下问题:
⑴测量氢气体积的正确装置是___________(填写编号)。
⑵装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是_________(填写编号)。
A. 防止无水酒精挥发 B. 保证实验装置不漏气 C. 使无水酒精容易滴下
⑶如果将此实验的数据视作标准状况下的数据,无水酒精的密度为ρg/cm3,VmL酒精反应完全后,量筒内的液面读数为M mL,则乙醇分子中能被钠取代出的氢原子数为__________________________。
⑷若实验所测定的结果偏高,可能引起的原因是__________(填写编号)。
A. 反应速率太快 B. 无水酒精中混有少量水
C. 读数时量筒内的液面高于广口瓶内的液面
五、计算题(共16分)
30、(5分)如右图,在试管甲中先加入2mL无水乙醇,并在摇动下缓缓加入2mL
浓硫酸,充分摇匀,冷却后再加入2 g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管乙中加入5mL饱和碳酸钠溶液。按右图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。试回答:
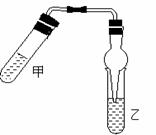 (1)试管乙中观察到的现象是
(1)试管乙中观察到的现象是
(2)加入浓硫酸的目的是:
(3)该实验使用球形管除去冷凝作用外,另一重要作
用是
(4)试管乙中饱和碳酸钠溶液的作用是:
_________________________________________
40.有一元羧酸和一元醇形成的酯A。燃烧0.1mol A,可得到5.4g H2O和6.72L CO2(标准状况下)。3.7g A与100ml某浓度NaOH溶液共热,当完全水解后,为中和剩余的NaOH,需消耗0.5mol/L盐酸60ml。求:
(1) A的分子式。
(2) A在酸性条件下水解后的两种产物的相对分子质量相等,写出A的结构简式。
(3) NaOH溶液的物质的量浓度。
39.有铁、铝混合物16.6g,将它跟足量的稀盐酸反应,得到11.2L氢气(标准状况)。求混合物中铁的质量。
38.为了在实验室制取乙酸乙酯,甲、乙、丙三个学生分别设计了下列装置:
(1)实验装置与所用药品都正确的是(用“甲”、“乙”或“丙”表示) ▲
(2)如果用含氧的同位素18O的乙醇跟乙酸起反应,写出该反应的化学方程式(标出产物中的18O) ▲
(3) 反应结束后,试管A内的液体分成两层,反应生成的乙酸乙酯在 ▲ 层(填写“上”或“下”)
37.有A、B、C、D4种溶液,其中阳离子分别为Ag+、Ba2+、Al3+、Fe3+,阴离子分别为Cl-、NO3-、OH-、SO42-。4种溶液中阴阳离子都不重复。现进行如下实验:
(1)在C溶液中加入铁粉,溶液质量增加;
(2)在A溶液中滴入酚酞试液,溶液呈红色;
(3)在B溶液逐滴滴入过量氨水时,先出现沉淀,后沉淀逐渐消失;
(4)在B和D溶液中分别加入硝酸钡溶液,均无明显现象。
由上述现象可推知各种溶液中溶质的化学式分别是:
A ▲ ,B ▲ ,C ▲ ,D ▲
36.将5.1g镁铝合金溶于60ml 5.0mol/LH2SO4溶液中,当合金完全溶解后,再加入65ml 10.0mol/L的NaOH溶液,得到沉淀的质量为9.7g。继续滴加NaOH溶液,沉淀质量减少,则合金溶于硫酸时产生H2的物质的量为 ▲ mol
35.有机物A的分子式为C9H10O2,在一定条件下能发生下列一系列变化 :
已知:D是最简单的有机物;E能与NaOH溶液反应;F转化为G时的产物只有一种,且该产物能跟溴水反应。写出A的结构简式 ▲
34.已知A、B、C、D分别是AlCl3、Ba(NO3)2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
已知:
①A+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
②C+D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失
请写出A、B、C的化学式:A ▲ 、B ▲ 、C ▲
33、写出下列反应的化学方程式
(1)苯跟溴的取代反应(铁作催化剂) ▲
(2)乙醛跟新制的氢氧化铜混合加热至沸腾 ▲
(3)氧化铝跟氢氧化钠溶液反应(写离子方程式) ▲
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com