
题目列表(包括答案和解析)
20.计算题将V ml NO和NO2的混合气体通过足量水吸收后,得到 a ml 无色气体A ,将A与等体积O2混合,再通过水充分吸收后,收集到5 ml 无色气体B 。
试回答:(1)A、B各为何种气体? (2)A气体的体积是多少?
(3)V的取值是多少?
19.现有原子序数之和为51的五种短周期元素A、B、C、D、E。已知A单质在常温下为无色气体;B原子的最外层电子数比次外层多了3个;C和B属于同族元素;D的最高正价和负价的代数和为4,其氢化物的熔点在同主族元素的氢化物中最低,E元素的原子最外层电子数与其K层电子数相同。
写出它们的元素符号:A __ 、B 、C 、D 、E 。
18.红磷在露置情况下久存往往表面发潮,这是由于红磷在空气中表面极缓慢地氧化,生成P2O5有吸水性,形成粘稠状液体所致,要得到干燥的红磷最好的办法是________.
A.加热使其挥发掉 B.水洗除去易溶的粘稠液体,立即干燥密闭保存
C.加石灰干燥后再水洗、过滤、干燥、密封保存
D.加还原剂使其还原为红磷,再干燥、密封
17. 汽车尾气(含有CO、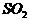 与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转化器”,它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使
与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转化器”,它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使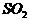 的转化。
的转化。
(1)写出CO与NO反应的化学方程式_____________________。
(2)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是__________。
(3)控制城市空气污染源的方法可以有_________。
a. 开发氢能源 b. 使用电动车 c. 植树造林 d. 戴呼吸面具
16.在适当的温度和压力下,4体积某气态氢化物完全分解后,产生1体积的磷蒸气和6体积的氢气.由此可以推断该气态化合物的分子式为________;该分解反应的化学方程式为_____________________________________________.
15.有两种气体,一种能氧化氮气,一种能还原氮气.写出这两个反应的化学方程式:
(1)________________________________;(2)_________________________________.
14.1999年曾报道合成和分离了含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是 A、N5+共有34个核外电子 B、N5+中氮原子之间以共用电子对结合
C、N5AsF6中As的化合价为+1 D、 N5AsF6中F的化合价为-1
13.将H2、N2、O2三种气体分别放入不同容器中,使它们的温度、密度相同,则其压强(p)大小的关系,符合(原子量:H 1 N 14 O 16)
A.p(H2)>p(O2)>P(N2) B. p(O2)>P(N2)>p(H2)
C.p(H2)>P(N2)>p(O2) D. P(N2)>p(O2)>p(H2)
12.常温下将盛有10mL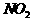 和10mL
和10mL 混合气体的试管倒立于水中,并向其中通入
混合气体的试管倒立于水中,并向其中通入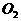 一段时间后,试管内剩余2mL气体,则通入
一段时间后,试管内剩余2mL气体,则通入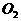 的体积为
的体积为
A. 8mL B. 8.5mL C. 10mL D. 12mL
11.科学家用计算机模拟后确认,60个N原子可结合成N60分子。下列关于N60的叙述中正确的是
A. N60是一种新型的化合物 B. 一个N60分子中含有30个N2分子
C. N60和N2的性质完全相同 D. N60和N2混合形成的是混合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com